活性芳香環・不活性芳香環の臭素化:NBSを用いた臭素化反応②:N-ブロモ化合物④:臭素化・ヨウ素化反応解説シリーズ 4
マナックが得意とする、臭素化・ヨウ素化反応について解説する本シリーズ。前回からは、NBSを使用したさまざまな臭素化反応を解説しています。
今回ご紹介するのは、「芳香環の臭素化」です。NBSを使用すれば、電子供与基で活性化された芳香環はもちろんのこと、電子求引基で不活性化された芳香環も反応条件次第では臭素化できます。反応の原理や溶媒効果、反応例などを解説しますので、ぜひ本記事の内容を参考にしてください。
■ この記事でわかること ✔ NBS中の臭素原子は正に分極しており、電子が豊富な化合物に対して求電子的に作用する ✔ 臭素化反応の位置選択性は溶媒の極性に著しく依存する ✔ 従来技術では解決できない反応上の課題を克服するため、マナックではマイクロフロー合成の研究を進めている ■ おすすめ記事 ・ アルケンの臭素付加やブロモヒドリン化、アルコールからブロモアルカンの合成:NBSを用いた臭素化反応③:N-ブロモ化合物⑤:臭素化・ヨウ素化反応解説シリーズ 5 ・ アリル位およびベンジル位の臭素化:NBSを用いた臭素化反応①:N-ブロモ化合物③:臭素化・ヨウ素化反応解説シリーズ 3
contents
N-ブロモスクシンイミド(NBS)とは
取り扱いが容易で、非常によく使用される臭素化剤
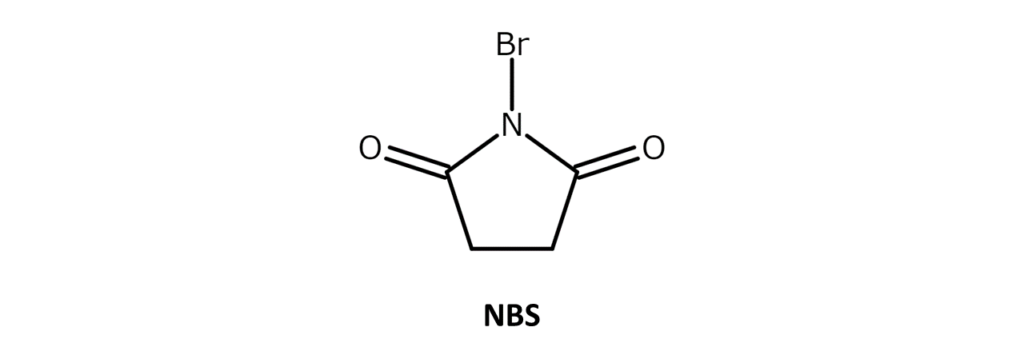
NBSは弱い臭素臭をもつ白~微黄色の結晶性粉末で、融点は173~176℃(分解)。アセトン、THF、DMF、アセトニトリル、DMSOなどに可溶で、水や酢酸には微溶、ヘキサンや四塩化炭素には難溶の化合物です。
粉末状で、臭素(液体)と比べて取り扱いが容易なため、有機合成では臭素化剤の第一選択としてよく使用されます。乾いた冷暗所で長期的に保存でき、値段も比較的安価です。
NBSの特徴や注意点、NBSを使用した臭素化反応の概要などに関しては、こちらの記事をご覧ください。
NBSを用いた臭素化反応:活性芳香環の臭素化
反応の詳細
NBS中の窒素原子は、電子求引性のカルボニル基と隣接しています。そのため、NBS中の臭素原子は正に分極しており、電子が豊富な化合物に対して求電子的に作用します。
今回ご紹介する「活性芳香環の臭素化」は、NBSが「電子供与基で『中程度に』活性化された芳香環」や「電子豊富なヘテロ芳香環」に対して求電子的に作用し、これらを臭素化する反応です(芳香族求電子置換反応)。
本反応が円滑に進行するには、電子供与基による芳香環の活性化度合いが「中程度」であることが重要です。芳香環がヒドロキシ基やアミノ基といった強力な活性化基で「過度に」活性化されている場合、NBSの作用で酸化や樹脂化を受けやすくなってしまうのです。しかしこのような場合であっても、ヒドロキシ基やアミノ基をエステル基やアミド基に変えて保護すれば、大抵はうまく臭素化できます。
臭素化反応の位置選択性は、溶媒に大きく支配されます。クロロ基やニトロ基などのような不活性基をもつ3-置換アニリンを、NBSを用いてさまざまな反応溶媒の下で臭素化した結果2)を下表に示します。この結果から、反応の位置選択性は溶媒の極性に著しく依存することがわかります。
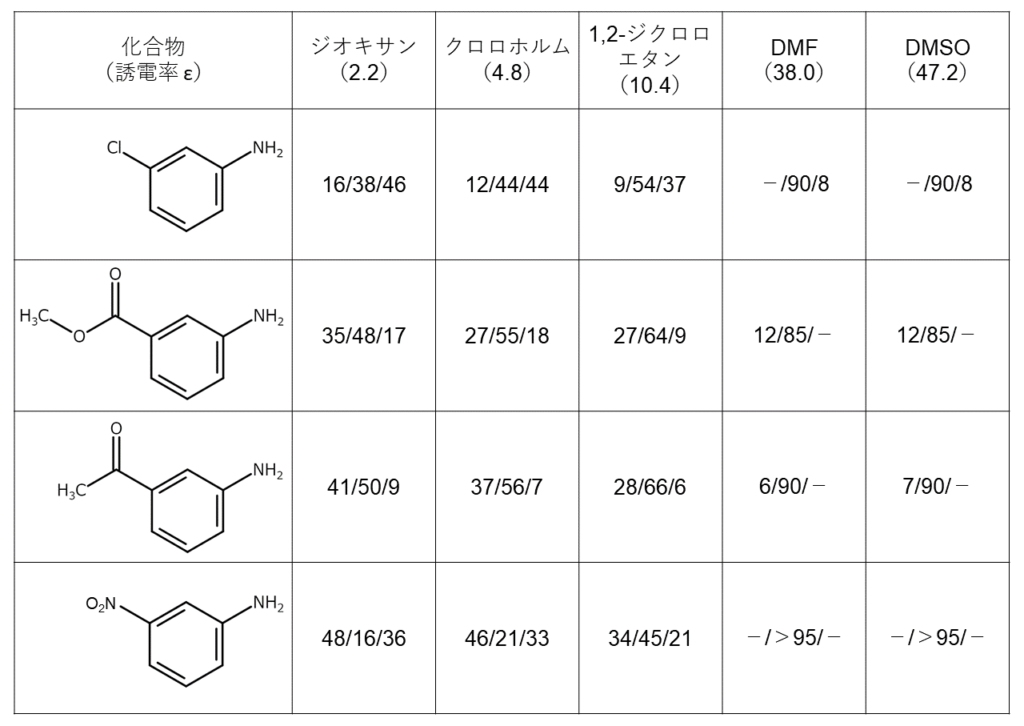
数字は、左から順に2,4および6位の臭素化物の異性体比を示す。
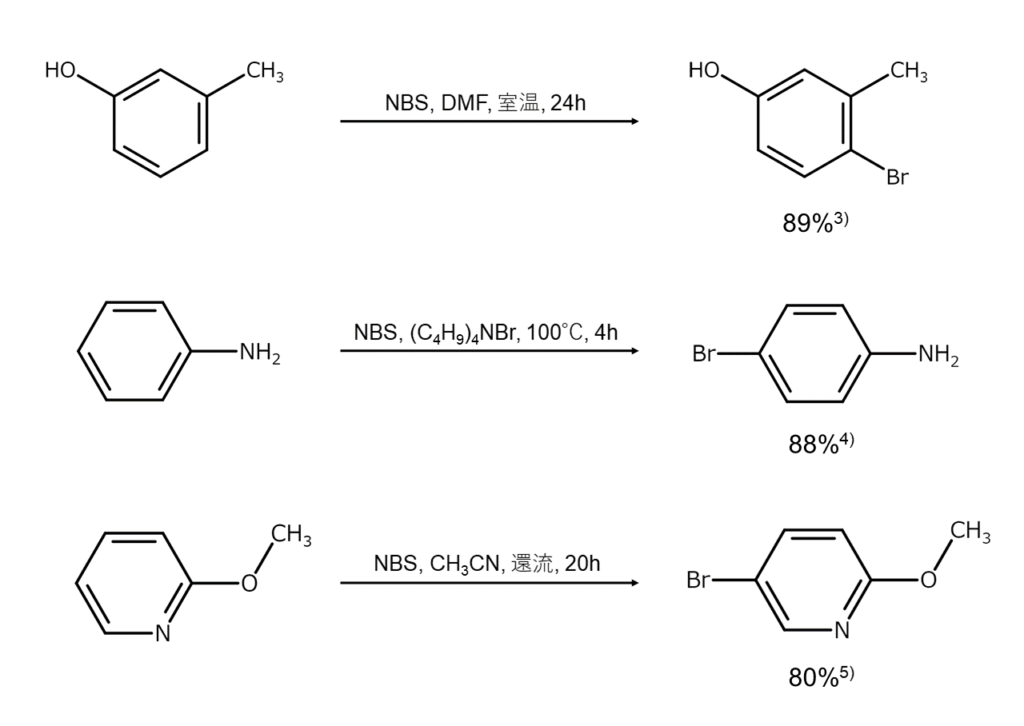
以下に、NBSを用いた活性芳香環の臭素化反応をいくつか示します。
【マナックこぼれ話】マイクロフロー合成で臭素化反応の位置選択性を制御する
活性芳香環の臭素化は温和な条件でも進行するため、大抵の場合、反応の進行条件を比較的容易に見つけることができます。ただし、活性な芳香環上に反応点(臭素化可能な位置)が複数ある場合は話が別です。このような芳香環上の特定の位置のみを選択的に臭素化するためには、臭素化剤や溶媒の種類や量、反応温度や添加方法などの細かな条件設定が必要となります。検討の結果、目標の反応選択性には届かないケースも、当然あります。
臭素化反応に限らず、従来技術では解決できない反応上の課題を克服するため、マナックではマイクロフロー合成の研究を進めています。
NBSを用いた臭素化反応:不活性芳香環の臭素化
反応の詳細
電子求引基で不活性化された芳香環はNBSによる求電子置換反応が起こりにくい状態であり、温和な条件では臭素化はほとんど進行しません。しかし、硫酸を溶媒に用いれば臭素化が可能です。
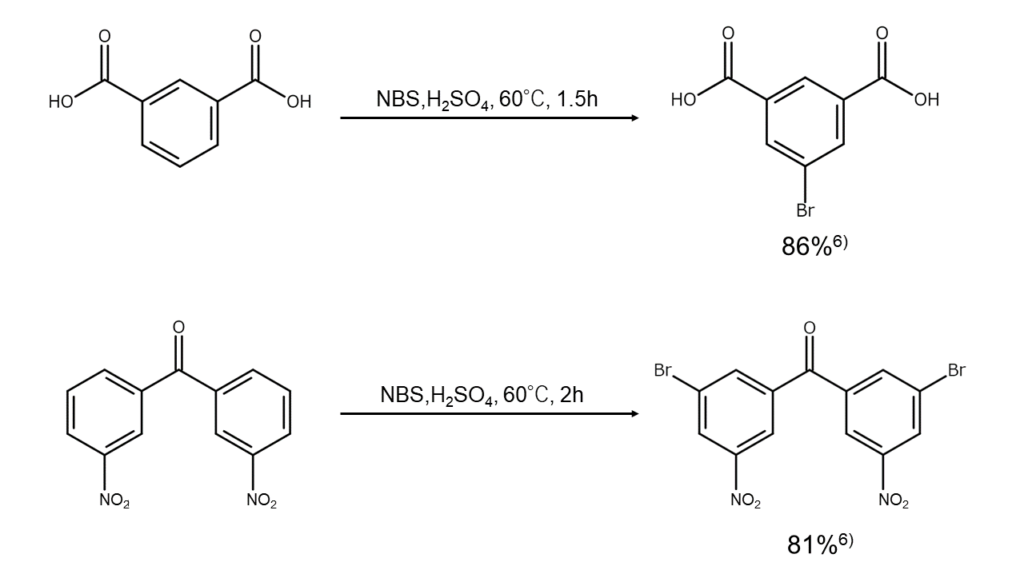
以下に、NBSを用いた不活性芳香環の臭素化反応をいくつか示します。
【マナックこぼれ話】溶媒である硫酸はどう処理するのか?
強い不活性化基であるニトロ基を有する不活性芳香環の臭素化は、m(メタ)位に臭素を導入できるため、合成上は非常に有用です。しかし工業的な観点からは、手放しでは歓迎できない反応でもあります。なぜなら、「反応溶媒として大量に使用した硫酸を反応後にどう処理するのか?」という問題が常について回るからです。工業的な反応設計においては、溶媒の廃棄方法などを含めた総合的な検討が必要なのです。
マナックは、代表的なN-ブロモ化合物であるNBSおよびDBDMHを製造・販売しています。ぜひ、お気軽にお問い合わせください。
参考文献
1) 鈴木仁美 監修、マナック(株)研究所 著、「臭素およびヨウ素化合物の有機合成 試薬と合成法」、丸善出版
2) Bartoli, S., Cipollone, A. et al. Synthesis, 2009, 1305.
3) Mitchell, R. H., Lai, Y.-H. et al. J. Org. Chem., 1979, 44, 4733.
4) Ganguly, N. C., De, P. et al. Synthesis, 2005, 1103.
5) Canibano, V., Rodriguez, J. F. et al. Synthesis, 2001, 2175.
6) Rajesh, K., Somasundaram, M. et al. J. Org. Chem., 2007, 72, 5867.