アリル位およびベンジル位の臭素化:NBSを用いた臭素化反応①:N-ブロモ化合物③:臭素化・ヨウ素化反応解説シリーズ 3
マナックが得意とする、臭素化・ヨウ素化反応について解説する本シリーズ。今回からは、NBSを使用したさまざまな臭素化反応を取り上げます。
今回の記事で解説するのは、NBSを用いる反応の代表格とも言える「アリル位およびベンジル位の臭素化」です。反応の原理や注意点、反応例などをご紹介しますので、ぜひ参考にしてください。
■ この記事でわかること ✔ NBSの代表的な反応に、アリル位やベンジル位の臭素化がある ✔ 臭素化反応と脱臭素化反応を組み合わせることで、一臭素化された化合物を選択的に得られる場合もある ✔ マナックは、代表的なN-ブロモ化合物であるNBSおよびDBDMHを製造・販売している ■ おすすめ記事 ・ 活性芳香環・不活性芳香環の臭素化:NBSを用いた臭素化反応②:N-ブロモ化合物④:臭素化・ヨウ素化反応解説シリーズ 4 ・ ベンジル位の臭素化、芳香環の臭素化:DBDMHを用いた臭素化反応:N-ブロモ化合物⑨:臭素化・ヨウ素化反応解説シリーズ 9 ・ 酸性や塩基性の特性を与える/「α-ブロモ化合物」シリーズ
contents
N-ブロモスクシンイミド(NBS)とは
取り扱いが容易で、非常によく使用される臭素化剤
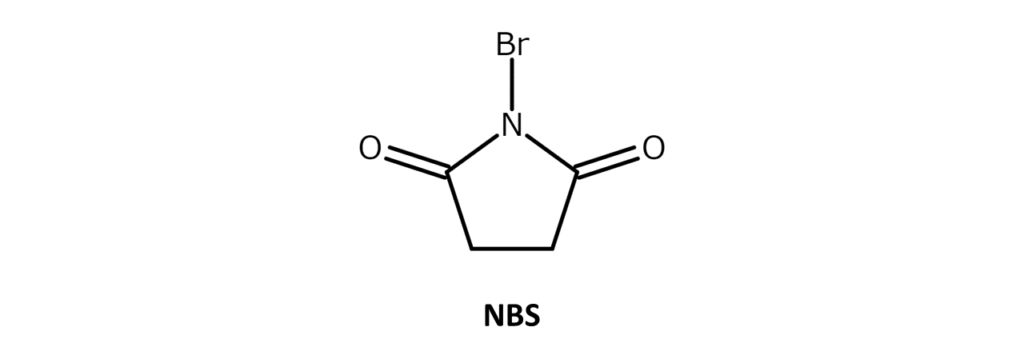
NBSは弱い臭素臭をもつ白~微黄色の結晶性粉末で、融点は173~176℃(分解)。アセトン、THF、DMF、アセトニトリル、DMSOなどに可溶で、水や酢酸には微溶、ヘキサンや四塩化炭素には難溶の化合物です。
粉末状で、臭素(液体)と比べて取り扱いが容易なため、有機合成では臭素化剤の第一選択としてよく使用されます。乾いた冷暗所で長期的に保存でき、値段も比較的安価です。
NBSの特徴や注意点、NBSを使用した臭素化反応の概要などに関しては、こちらの記事をご覧ください。
NBSを用いた臭素化反応:アリル位およびベンジル位の臭素化
反応の詳細
アリル位やベンジル位の臭素化は、NBSの代表的な反応です。この反応はWohl-Ziegler反応ともよばれ、ラジカル連鎖的に進行します。
アリル位の臭素化を例として、以下に反応機構を示します。最初に、NBS中のN-Br結合がラジカル的に開裂し、発生したBrラジカルがアリル位の臭素に結合した水素原子を引き抜くことで、アリルラジカルとHBrが発生します。このHBrは別のNBSと反応し、in situでBr2が発生します。このBr2が先ほどのアリルラジカルと反応して、アリル位が臭素化されるのです。臭素化の過程で別のBrラジカルが生成されるため、ラジカル連鎖的に反応が起こります。
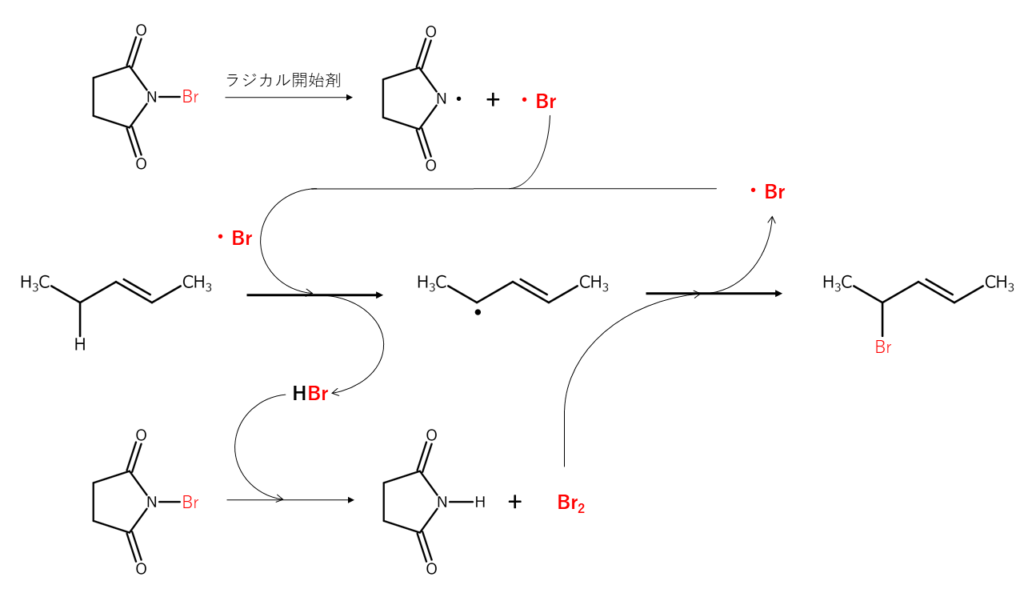
上記の臭素化反応は、CH2(第二級炭素)>CH3(第一級炭素)>CH(第三級炭素)の順に起こりやすいことが知られています。反応の進行が遅い場合には、ラジカル発生剤(5~10%)の添加や光照射が有効なケースもあります。反応に使用する溶媒は、四塩化炭素やベンゼン、シクロヘキサンなどです。溶媒も臭素化の選択性に影響をおよぼすため2)、反応を設計する際には溶媒効果も考慮しましょう。
また、同じN-ブロモ化合物であるN-ブロモフタルイミドもアリル位の臭素化に利用できます。しかし、反応性が低いなどの理由で、NBSと比べて合成上の利点はあまりありません。
以下に、NBSを用いたアリル位およびベンジル位の臭素化反応の例を示します。
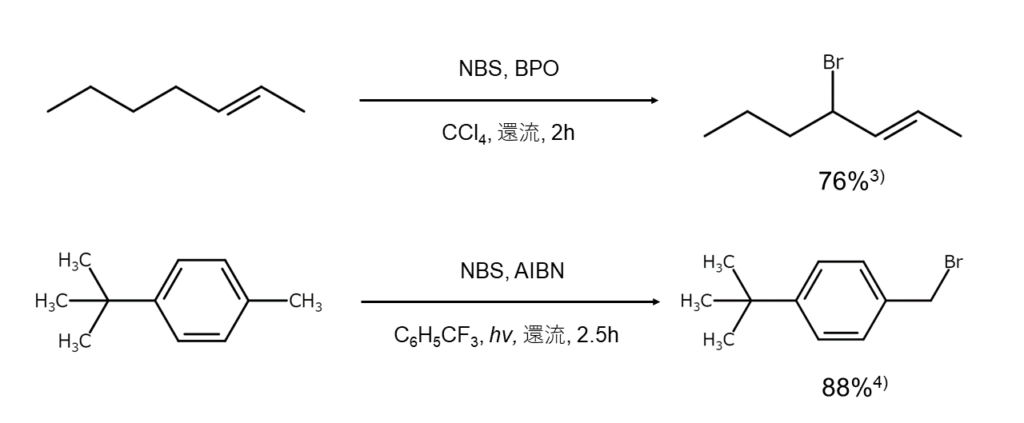
一臭素化された化合物を選択的に得ることも可能
臭素化反応と脱臭素化反応を組み合わせることで、一臭素化された化合物を選択的に得られる場合もあります。例えば、ラジカル開始剤の共存下で過剰のNBSを用いてベンジル位を多臭素化した後、亜リン酸ジエチルとN,N-ジイソプロピルエチルアミンで還元的に脱臭素すると、以下のようにベンジル位が一臭素化された化合物のみが選択的に得られます5)。
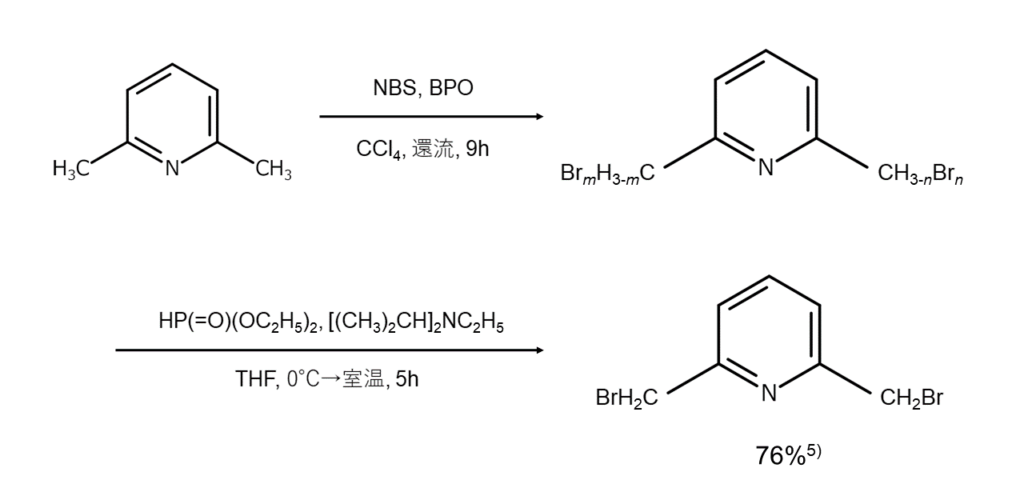
以下に、ベンジル位を選択的に一臭素化する反応の例を示します。

【マナックこぼれ話】アリルブロミドやベンジルブロミドは取り扱いに注意!
アリル位やベンジル位の臭素化反応で生成する「アリルブロミド」や「ベンジルブロミド」は、反応性が高い臭素化合物で、中間体としてよく利用されます。一方で、これらの化合物が皮膚に付着したり、これらの化合物の蒸気を吸い込んだりしてしまうと、体質によっては発疹などの症状が現れることもあります。さらに、揮発性の高い化合物の場合、実験室で少量取り扱うだけで眼の痛みや皮膚への刺激を感じることもあるため、注意が必要です。
アリルブロミドやベンジルブロミドを目的物として合成する場合はもちろん、副生物としてこれらの化合物が生成し得る場合にも、ドラフト内で作業する、保護具を着用するなどの対策を講じる必要があります。
マナックは、代表的なN-ブロモ化合物であるNBSおよびDBDMHを製造・販売しています。ぜひ、お気軽にお問い合わせください。
参考文献
1) 鈴木仁美 監修、マナック(株)研究所 著、「臭素およびヨウ素化合物の有機合成 試薬と合成法」、丸善出版
2) Offermann, W,. Vogtle, F. Angew. Chem. Internat. Ed., 1980, 92, 471.
3) Greenwood, F. L., Kellert, M. D. J. Am. Chem. Soc., 1953, 75, 4842.
4) Suarez, D., Laval, G. et al. Synthesis, 2009, 1807.
5) Liu, P., Chen, Y. et al. Synthesis, 2001, 2078.