カルボニル基のα位の臭素化、カルボン酸と関連化合物の臭素化:NBSを用いた臭素化反応④:N-ブロモ化合物⑥:臭素化・ヨウ素化反応解説シリーズ 6
マナックが得意とする、臭素化・ヨウ素化反応について解説する本シリーズ。NBSを使用したさまざまな臭素化反応を解説しています。
今回ご紹介するのは、「カルボニル基のα位の臭素化」「カルボン酸と関連化合物の臭素化」です。カルボニル基やカルボン酸のα位を選択的に臭素化したり、カルボン酸を脱炭酸して臭化物に変えたりする反応を扱います。反応機構や反応例を解説しますので、ぜひ研究や実験の参考にしてください。
■ この記事でわかること ✔ NBSを用いることで、カルボニル基やカルボン酸のα位を選択的に臭素化できる ✔ NBSはHell-Volhard-ZelinskyやHunsdiecker反応の代替法として、穏やかな条件下で臭素化反応を効率よく進められる ✔ NBSは脱炭酸反応にも利用でき、カルボン酸を臭化物やブロモアルケンへ変換する際に適している ■ おすすめ記事 ・ プロパルギルアルコールからブロモアレンの合成、芳香環のオルト選択的な臭素化:NBSを用いた臭素化反応⑤:N-ブロモ化合物⑦:臭素化・ヨウ素化反応解説シリーズ 7 ・ アルケンの臭素付加やブロモヒドリン化、アルコールからブロモアルカンの合成:NBSを用いた臭素化反応③:N-ブロモ化合物⑤:臭素化・ヨウ素化反応解説シリーズ 5
contents
N-ブロモスクシンイミド(NBS)とは
取り扱いが容易で、非常によく使用される臭素化剤
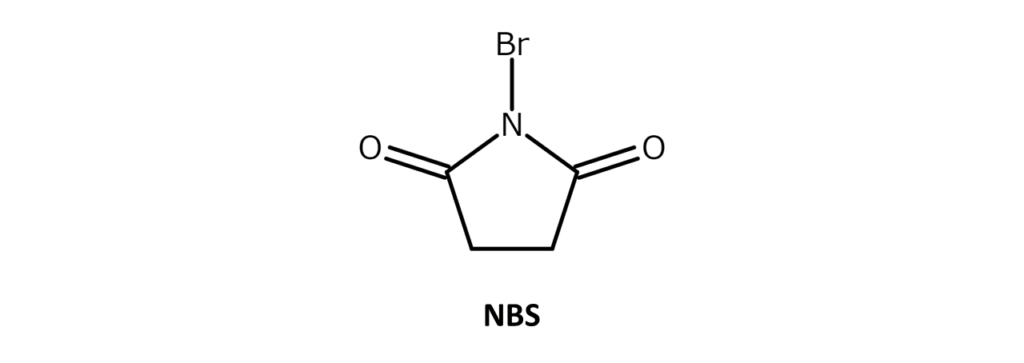
NBSは弱い臭素臭をもつ白~微黄色の結晶性粉末で、融点は173~176℃(分解)。アセトン、THF、DMF、アセトニトリル、DMSOなどに可溶で、水や酢酸には微溶、ヘキサンや四塩化炭素には難溶の化合物です。
粉末状で、臭素(液体)と比べて取り扱いが容易なため、有機合成では臭素化剤の第一選択としてよく使用されます。乾いた冷暗所で長期的に保存でき、値段も比較的安価です。
NBSの特徴や注意点、NBSを使用した臭素化反応の概要などに関しては、こちらの記事をご覧ください。
NBSを用いた臭素化反応:カルボニル基のα位の臭素化
反応の詳細
最初に紹介するのは、カルボニル基のα位を選択的に臭素化する反応です。この反応機構は、酸触媒を使用した場合と塩基触媒を使用した場合とで異なります。
酸触媒を使用した場合、最初に反応物がエノール化し、次いで求電子剤であるNBSが二重結合を攻撃して、中間体であるハロカルボカチオンが生じます。その後、ハロカルボカチオンが脱プロトン化して臭素化が完了します。この反応は、最初の臭素が導入されたところで停止するのがふつうです。一方で塩基触媒を使用すると、α位が完全に臭素化するまで反応が続きます。
以下に、酸触媒を使用した場合の反応機構を示します。
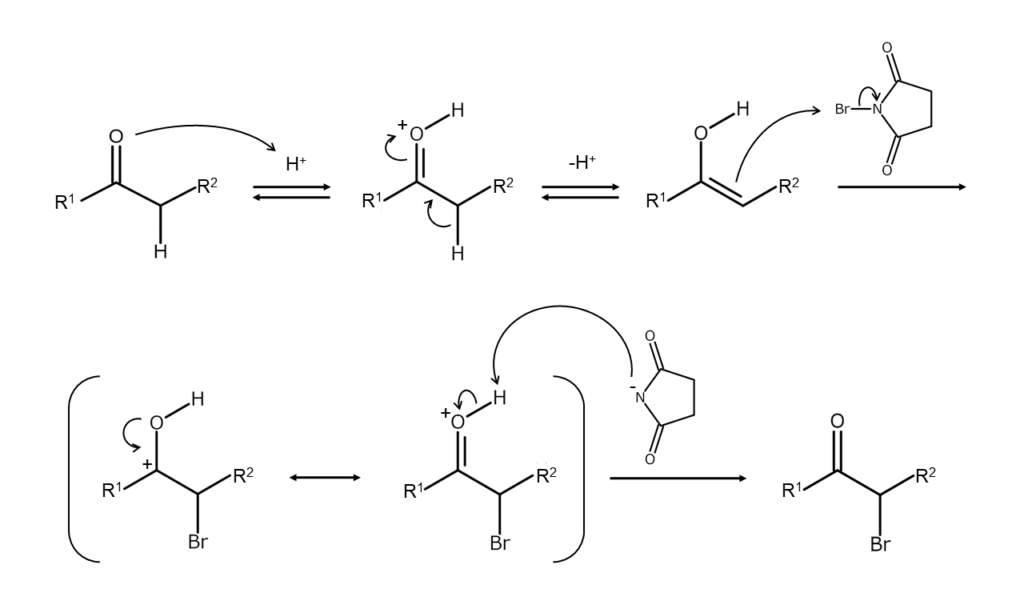
また、炭酸カリウムの存在下でα,β-不飽和カルボニル化合物をNBS-(C2H5)3N・3HBrで臭素化すると、不飽和結合のα位を選択的に臭素化できます。
以下に、NBSを用いてカルボニル基のα位を臭素化する反応の例を示します。
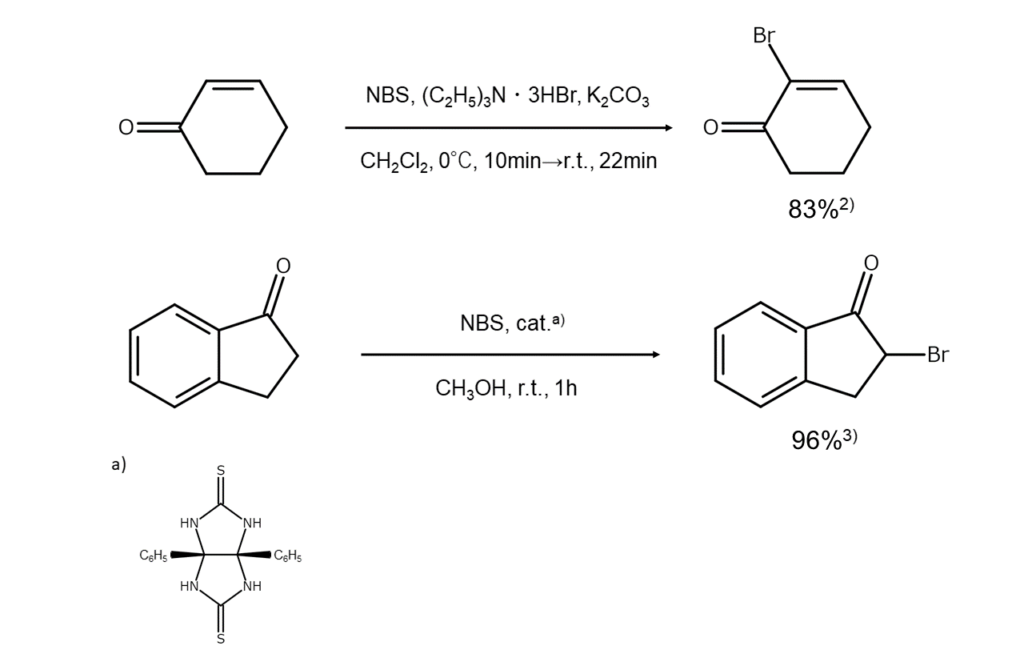
非対称ケトンを反応物とする場合、シリルエノールエーテルに変えてエノール化の方向を固定すれば、穏やかな条件下で一方のモノブロモケトンのみを特異的に合成できます。この反応例を以下に示します。
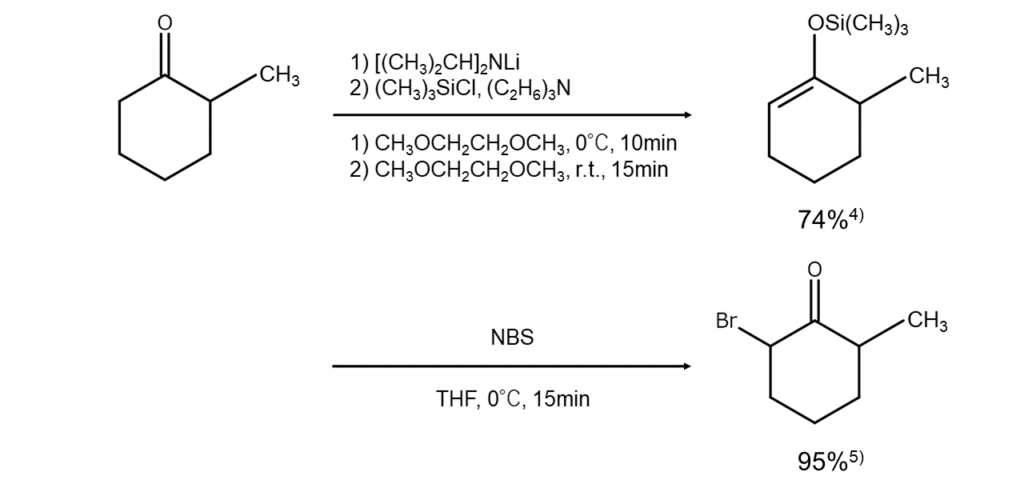
NBSを用いた臭素化反応:カルボン酸と関連化合物の臭素化
反応の詳細
ここでご紹介するのは、「カルボン酸のα位を臭素化する方法」と「カルボン酸を脱炭酸して臭化物に変える方法」です。これらの反応はNBSを使用しない方法でも達成できますが、NBSを使用すればより有利な条件で進行します。以下では、従来の方法(NBSを使用しない方法)とNBSを使用する方法をそれぞれ解説します
①カルボン酸のα位を臭素化する方法
カルボン酸のα位を臭素化する方法としては、一般にHell-Volhard-Zelinsky反応6)7)8)が利用されてきました。これは、カルボン酸と少量の赤リンの混合物にBr2をゆっくり加えてPBr3を発生させた後、カルボン酸とPBr3の反応による臭化アシルの生成、臭化アシルのエノール化、エノールの臭素化、反応終了後の加水分解を経てα-ブロモカルボン酸を得る方法です。しかしHell-Volhard-Zelinsky反応には、高温で長時間の加熱を必要とする、収率にかなりの幅が見られるなどの欠点がありました。
上記欠点を解決する手段としては、塩化チオニル-四塩化炭素-HBrの反応系でカルボン酸塩化物をNBSと反応させる方法があります。この反応では、穏やかな加熱条件でα位を円滑に臭素化できます。反応の一般性が高く、ベンジル位が攻撃されない点もメリットです。
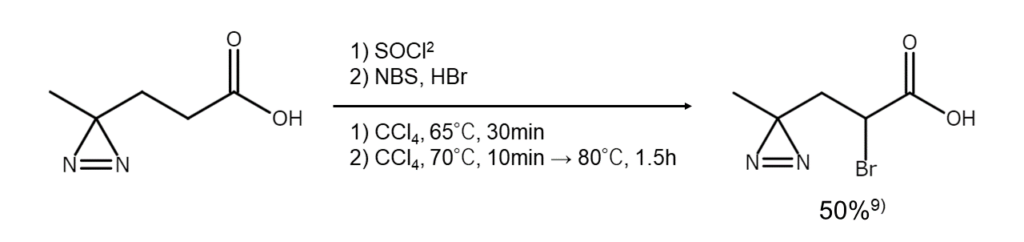
②カルボン酸を脱炭酸して臭化物に変える方法
カルボン酸を臭化物に変える方法として古くから有名なのは、Hunsdiecker反応10)11)。です。これは、カルボン酸の銀塩にBr2を反応させて臭化アルキルを合成する反応ですが、二重結合や活性メチレン基を有するカルボン酸にはうまく適用できない点が問題でした。
NBSをヨードシルベンゼンやテトラブチルアンモニウムトリフルオロアセタート(C4H9)4N+CF3CO2-と組み合わせれば、不飽和カルボン酸を効率よくブロモアルケンに変換できます。この方法を用いた不飽和カルボン酸の臭素化脱炭酸の反応例を、以下に示します。
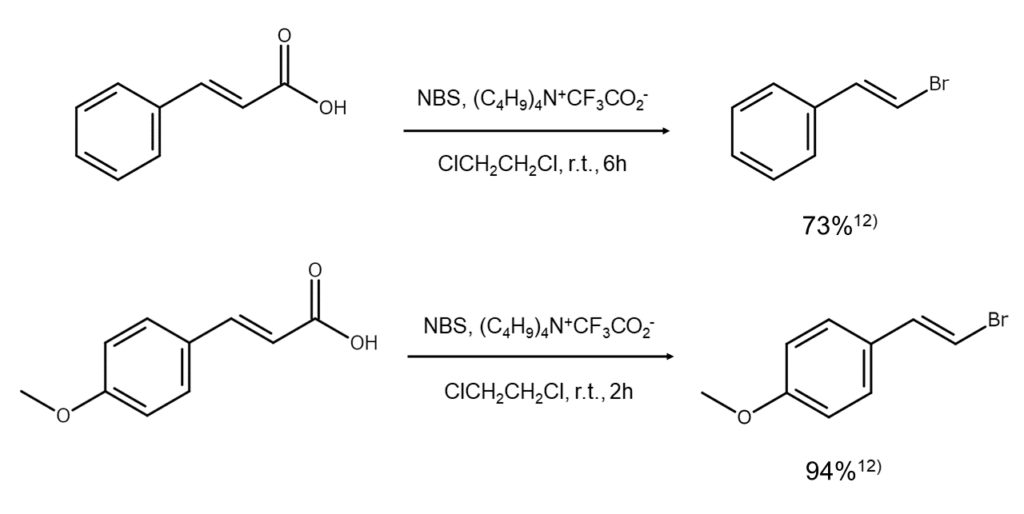
マナックは、代表的なN-ブロモ化合物であるNBSおよびDBDMHを製造・販売しています。ぜひ、お気軽にお問い合わせください。
参考文献
1) 鈴木仁美 監修、マナック(株)研究所 著、「臭素およびヨウ素化合物の有機合成 試薬と合成法」、丸善出版
2) Jyothi, D., HariPrasad, S. Synlett, 2009, 2309.
3) Cao, L., Ding, J. et al. Synlett, 2009, 1445.
4) House, H. O., Czuba, L. J. et al. J. Org. Chem., 1969, 34, 2324.
5) Reuss, R. H., Hassner, A. J. Org. Chem., 1974, 39, 1785.
6) Hell, C. Ber. Dtsch. Chem. Ges. 1881, 14, 891.
7) Volhard, J. Justus Liebig’s Ann. Chem. 1887, 242, 141.
8) Zelinsky, N. Ber. Dtsch. Chem. Ges. 1887, 20, 2026.
9) Ikeda, Y., Behrman, E. J., Synth. Commun. 2008, 38, 2276.
10) Borodine, A. Justus Liebigs Ann. Chem. 1861, 119, 121.
11) Hunsdiecker, H. et al., Ber. Dtsch. Chem.Ges. B 1942, 75, 291.
12) Naskar, D., Roy, S. Tetrahedron 2000, 56, 1369.