エーテルの開裂によるヨードアルカンの合成、ヨウ化アルカリを用いたその他の合成:ヨウ化アルカリを用いたヨウ素化反応③:臭素化・ヨウ素化反応解説シリーズ 26
ヨウ化ナトリウムやヨウ化カリウムに代表される「ヨウ化アルカリ」を用いたヨウ素化反応を取り上げてきた本シリーズ。いよいよ今回で、ヨウ化アルカリ編は最終回です。
本記事で主に取り上げるのは、エーテルやエポキシドを開裂させてヨードアルカンを合成する方法です。この反応を応用するには、エーテル酸素のどちら側にある官能基がヨウ素化されやすいかを理解しておく必要があります。今回は、その点も含めて反応機構をくわしく解説します。
このほか、本シリーズでくわしく扱えなかったその他のヨウ素化反応もダイジェストで紹介しています。ぜひ、最後まで目を通してみてください。
contents
ヨウ化アルカリを使用したヨウ素化反応:エーテルの開裂によるヨードアルカンの合成
求核置換反応によりヨードアルカンが生成する
酸触媒の存在下でエーテルにヨウ化アルカリを作用させると、エーテル結合が開裂してヨードアルカンが得られます。この反応は、エーテル酸素のプロトン化で発生したオキソニウムイオン中間体をヨウ素イオンが求核攻撃することで進みます。反応機構は以下のとおりです。
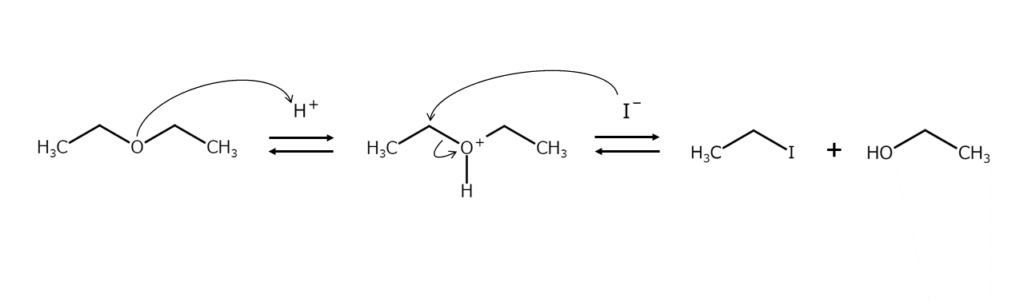
上記反応からは、どのような生成物が得られるのでしょうか。非対称ジアルキルエーテルを開裂させるとヨードアルカンの混合物が得られますが、通常は第一級ヨードアルカンが優先的に生成します。また、アリルエーテルやベンジルエーテル、第三級アルキルエーテルは安定なカルボカチオンを発生しやすいため、これらのアルキル基側で優先的にヨウ素化開裂が起こります。また、フェノールのアルキルエーテルは常にヨードアルカンのみを与えます。
反応試薬としてよく利用されるのは、適用範囲が広いNaI-リン酸です2)3)。しかし、反応性が高いアリルエーテルの開裂には、酢酸またはギ酸中でKIを用いる方法がより好結果を与えると言われています4)。アルコールをヨードアルカンへ変換するのによく利用されるNaI-クロロトリメチルシランも、エーテルやエステルのヨウ素化開裂に利用できます5)。
エーテルのヨウ素化開裂の反応例を以下に示します。
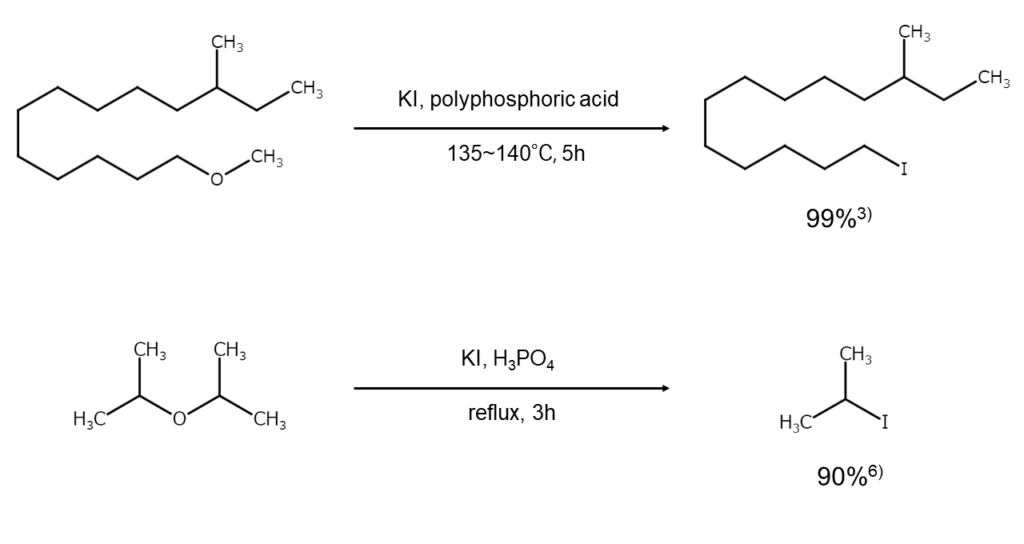
反応物がエポキシドである場合
エポキシドを開裂させるにはLiIの酢酸溶液が優れています。しかし、DMF、HMPAなどの非プロトン性溶媒中ではカルボニル化合物への異性化をともないやすいため、注意が必要です。また、エポキシドはMgI2のように穏やかなLewis酸でも開裂されて、ヨードヒドリンを与えます7)。
エポキシドのヨウ素化開裂の反応例を以下に示します。
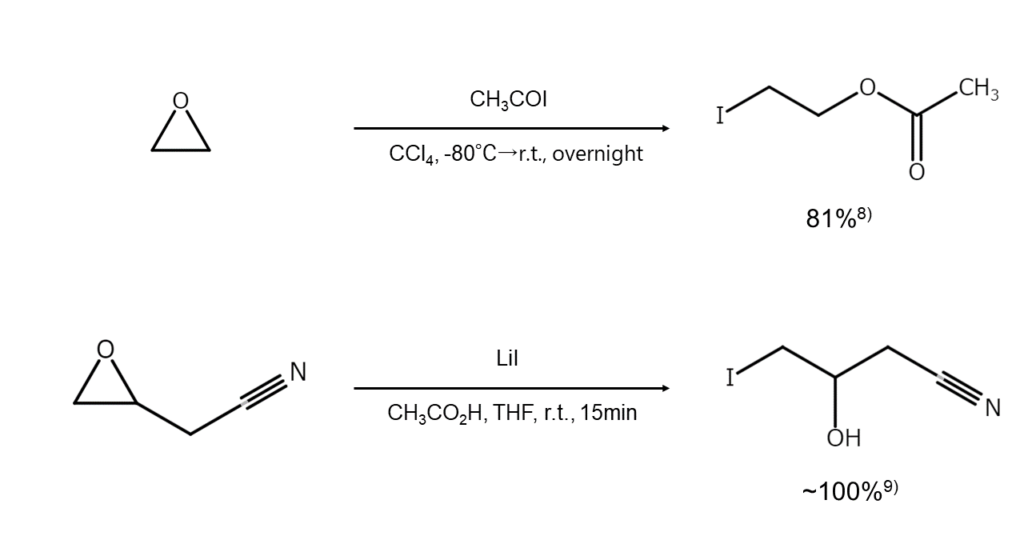
ヨウ化アルカリを使用したヨウ素化反応:ヨウ化アルカリを用いたその他の合成
ヨウ化アルカリを用いたヨウ素化方法は、ほかにもたくさん提案されています。ここでは、本シリーズでくわしく扱えなかったヨウ素化方法をダイジェストで紹介します。
① 有機ボランのヨウ素化開裂、フェノールのヨウ素化
NaIとクロラミン-Tの組み合わせは、有機ボランのヨウ素化開裂やフェノールのヨウ素化に利用されます。反応はin situに発生した一塩化ヨウ素IClによって起こりますが、IClを単独で使用した場合よりも好結果が得られます10)。なお、アルキルボランの開裂の容易さは第一級>第二級>第三級の順です。
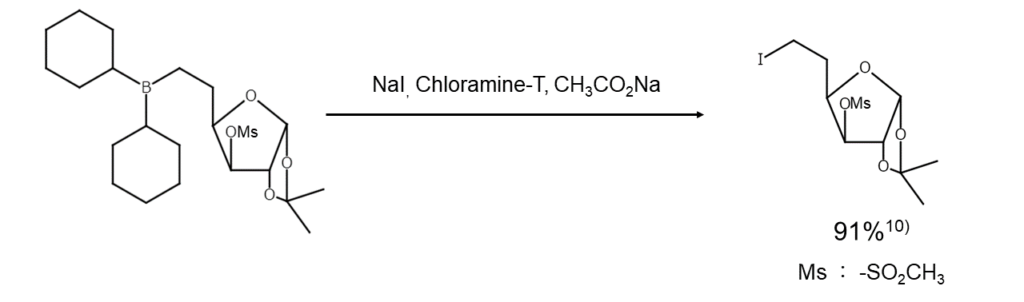
② 芳香環のヨウ素化
氷冷したメタノール中でフェノールにNaIとNaOCl水溶液を作用させると、発生した次亜ヨウ素酸イオンによって芳香環が容易にヨウ素化されます。生成物としては、試薬の量比に応じて、それぞれ4-ヨードフェノールが80%、2,4-ジヨードフェノールが78%、2,4,6-トリヨードフェノールが90%の収率で得られます11)。
③ ヨードニオ基のヨウ素化
オレフィン炭素上の置換基を求核的に置換するのは一般的に困難ですが、ヨードニオ基はヨウ素アニオンによって容易に置換されます。置換時には立体配置が反転しますが、β位にスルホニル基を導入すると立体化学が保持されます12)13)。
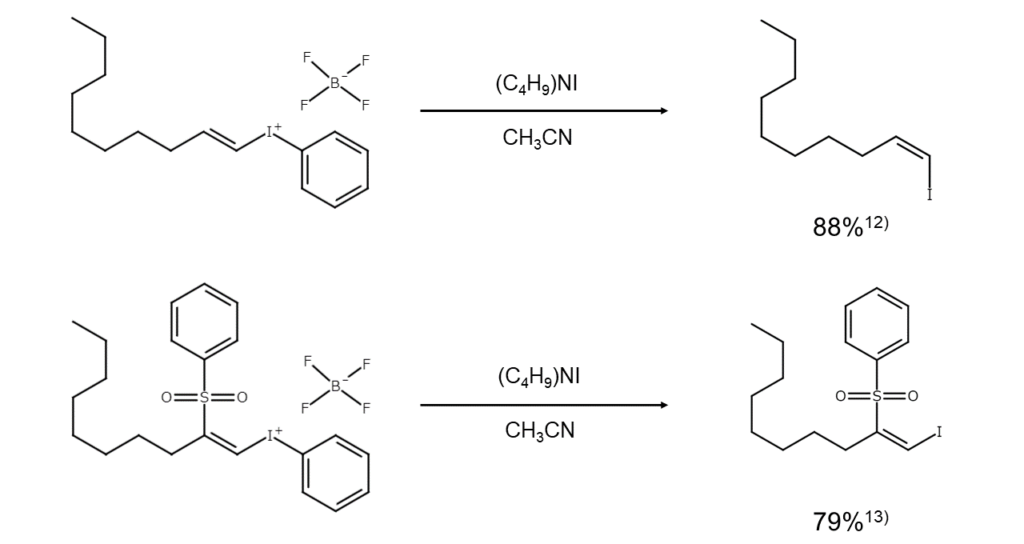
④ セレノンのヨウ素化開裂
スルホンをヨウ素イオンで開裂させることはできません。しかし、セレノンはすみやかに開裂して、セレノニル基がセレネン酸イオンとして脱離し、対応するヨウ化物を与えます14)。
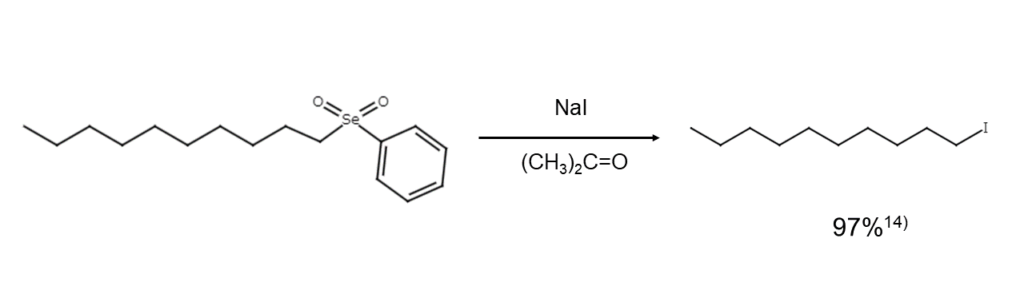
【コラム】昆虫のフェロモンとしても活躍するエポキシド
化学者のみなさんにとって、今回の記事に登場したエポキシドは「有機合成の現場で使われる化合物」というイメージが強いかと思います。しかし、実はエポキシドは生体内でも重要な役割を果たしているのです。その一例が、蛾類の性フェロモンとしての機能です。
蛾類は夜間に活動するため、視覚情報ではなく嗅覚情報を使って交尾や産卵を効率的に進めます。性フェロモンも、そんな嗅覚情報のひとつです。メスが分泌した性フェロモンをオスが触覚上の嗅覚受容器で検知することで、オスは広い空間からにおいの源であるメスを探し、交尾できるのです。
蛾類の性フェロモンには、脂肪族型(タイプI、原料:アセチルCoA)と炭化水素型(タイプII、原料:必須脂肪酸)の2種類があります15)。このうち、炭化水素型の性フェロモンを有する蛾類の6~7割が、エポキシドを性フェロモンとしています。近年、蛾の性フェロモン生合成におけるエポキシ化酵素の機能に関しても研究が進められています16)。
今回挙げた例以外にも、エポキシドはさまざまな形で生命活動に関与しています。興味がある方は、ぜひ一度調べてみてください。
参考文献
1) 鈴木仁美 監修、マナック(株)研究所 著、「臭素およびヨウ素化合物の有機合成 試薬と合成法」、丸善出版
2) Stone, H., Shechter, H. Org. Synth. Coll. Vol. IV, 321 (1963).
3) Cope, A. C., Burrows, E. P. et al. J. Am. Chem. Soc., 1965, 87, 5452.
4) Mustafa, A., Sidky, M. M. et al. Liebigs Ann. Chem., 1967, 704, 182.
5) Olah, G. A., Narang, S. C. et al. J. Org. Chem., 1979, 44, 1247.
6) Stone, H., Shechter, H. J. Org. Chem., 1950, 15, 491.
7) Otsubo, K., Inanaga, J. et al. Tetrahedron Lett., 1987, 28, 4435.
8) Belsner K., Hoffmann, H. M. R. Synthesis, 1982, 239.
9) Bajwa, J. S., Anderson R. C. Tetrahedron Lett., 1991, 32, 3021.
10) Kabalka, G. W., Gooch, E. E. J. Org. Chem., 1981, 46, 2582.
11) Edgar, K. J., Falling, S. N. J. Org. Chem., 1990, 55, 5287.
12) Ochiai, M., Oshima, K. et al. J. Am. Chem. Soc., 1991, 113, 7059.
13) Ochiai, M., Oshima, K. et al. Tetrahedron Lett., 1991, 32, 7711.
14) Krief, A., Dumont, W. et al. J. Chem. Soc., Chem. Commun., 1985, 571.
15) Ando, T., Inomata, S. et al. Topics in Current Chemistry, 2004, 239, 51.
16) 清水伸泰他、「昆虫のフェロモン2 脂肪酸に由来するフェロモンの生合成と受容機構」、https://www.jstage.jst.go.jp/article/kagakutoseibutsu/57/12/57_571208/_pdf