臭化水素を用いた臭素化反応(臭化水素と酸化剤を組み合わせた臭素化、臭化水素を用いたその他の合成):臭化水素⑤:臭素化・ヨウ素化反応解説シリーズ38
マナックが得意とする臭素化・ヨウ素化反応について解説する本シリーズは、過去4回にわたり臭化水素を用いたさまざまな臭素化反応を紹介してきました。ブロモアルカンの合成やアルケン・アルキンへの付加、ブロモメチル化など、臭化水素は多くの反応で活躍することが分かっていただけたかと思います。
そんな臭化水素による反応を取り上げるのも、今回でいよいよ最後。ラストを飾るのは、「臭化水素と酸化剤を組み合わせた臭素化反応」と、臭素原子の転位や臭素原子への置換について扱う「臭化水素を用いたその他の合成」です。
前者はin situで生成した単体臭素を臭素化剤とする方法で、反応を制御しやすく副反応が少ないといったメリットがあります。後者は、酸や熱の作用により転位反応や置換反応を引き起こす方法で、直接的な臭素化では得られない化合物の合成手段としても注目されています。臭素化反応を学ぶ上で、どちらもぜひ押さえておきたいトピックだと言えるでしょう。
この記事では、反応の原理や特徴などをまとめて解説します。ぜひ最後までご覧ください。
contents
臭化水素を用いた臭素化反応:臭化水素と酸化剤を組み合わせた臭素化
酸化剤の量によって反応を制御できる
臭化水素を適当な酸化剤と組み合わせて臭素Br2を発生させ、この臭素をin situに臭素化剤として利用することで、アルケンや芳香環などを臭素化できます。
この反応は臭素をごく低濃度に抑えた状態で実施できるため、活性化された基質の臭素化によく利用されます。また、酸化剤の量比で発生する臭素の濃度を制御できるため、単体臭素を直接作用させた場合に比べて副反応が少なく、好結果が得られる点も特徴です。
以下に示す4種の反応系が、アルケンや芳香環の臭素化、アルケンのブロモヒドリンへの変換によく利用されます。
HBr/DMSO系 (CH3)2SO + HBr → (CH3)2S + H2O + Br2
HBr/H2O2系 H2O2 + 2HBr → H2O + Br2
HBr/O2(hν)系 O2 + 4HBr + hν → H2O + Br2
HBr/NaNO2/O2系 2NaNO2 + 4HBr → 2NOBr + 2NaBr + H2O
2NOBr → 2NO + Br2
臭化水素と酸化剤を用いた臭素化の反応例を、以下に示します。
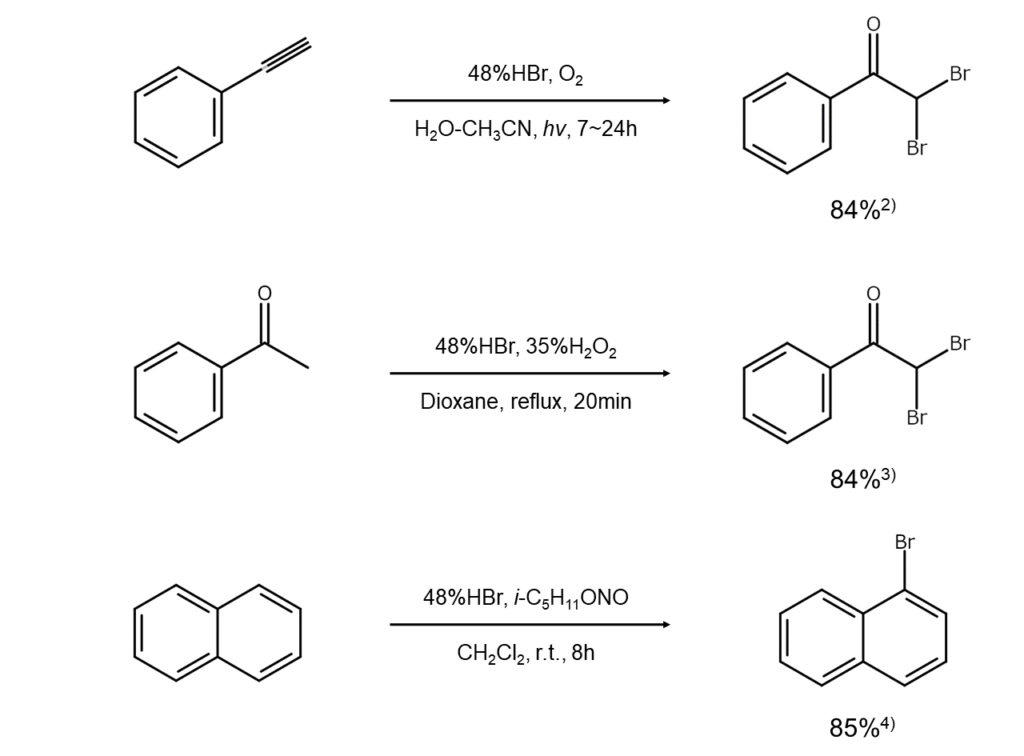
臭化水素を用いた臭素化反応:臭化水素を用いたその他の合成
芳香族臭素化合物における臭素転位反応
臭素化合物中のC-Br結合は、C-F結合やC-Cl結合に比べて弱く切断されやすいという特徴があります。そのため、C-Br結合が酸や熱、光などの作用で容易に切断され、生じた臭素原子が分子内外の他の場所に転位するケースがしばしば見受けられます。
このような臭素転位反応は、本記事のテーマである臭化水素によって引き起こされる場合もあります。以下は、活性化された芳香族臭素化合物に臭化水素酸を作用させて、臭素原子の分子内転位反応を起こした例です。

芳香族化合物中のニトロ基を臭素原子に置換する反応
続いて紹介するのは、置換反応によって臭素原子を新たに導入する反応です。活性化された位置にニトロ基を持つ芳香族化合物を濃い臭化水素酸と長時間加熱することで、ニトロ基を臭素原子に置換することができます。
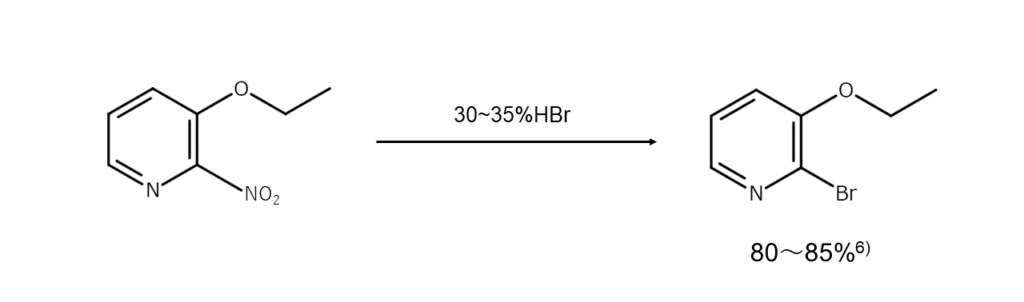
【コラム】臭素化合物の意外な合成法!? 臭素原子のさまざまな転位反応をご紹介
今回の記事では、「臭化水素を用いたその他の合成」として、臭化水素酸を用いた臭素の転位反応をご紹介しました。実は、このような転位反応は他のさまざまな条件下でも引き起こされます。「臭素化合物の特殊な合成法」とも言われるこれらの転位反応をいくつかご紹介しましょう。
濃硫酸やAl2Cl6と加熱する用いる方法
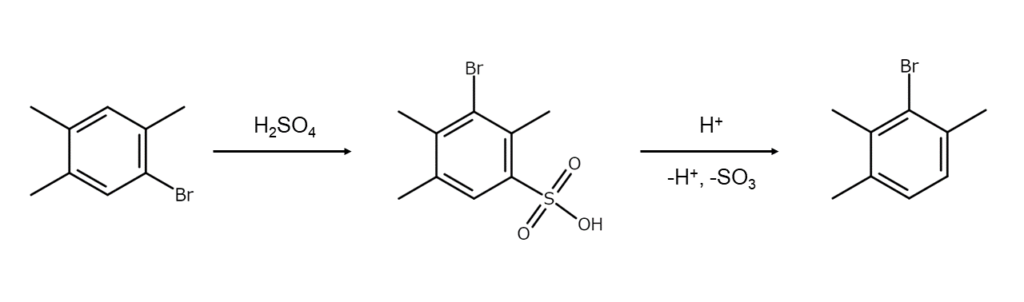
強い電子吸引基を持たない芳香族臭素化合物を濃硫酸やAl2Cl6と加熱すると、しばしば臭素原子が転位して異性体やポリブロモ化合物が生成します。よく知られているのは以下のJacobsen反応で、非隣接構造の臭素化合物を隣接構造の異性体に変える際に利用されます。
熱のみを利用する方法
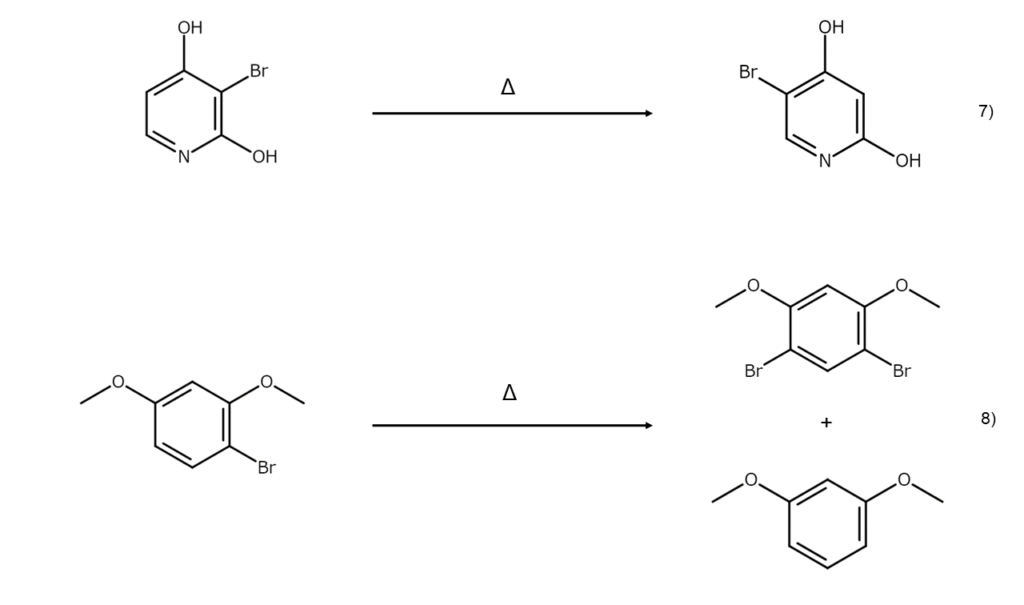
酸を用いなくても、熱だけで転位反応が進行するケースもあります。フェノール、レゾルシン、アニリンなどの臭素誘導体は、高温に加熱するだけでも異性化や部分的な不均化を起こして、別の臭素化合物へ変わりやすいことが知られています。
Al2Cl6とHClを含む二硫化炭素を用いる方法
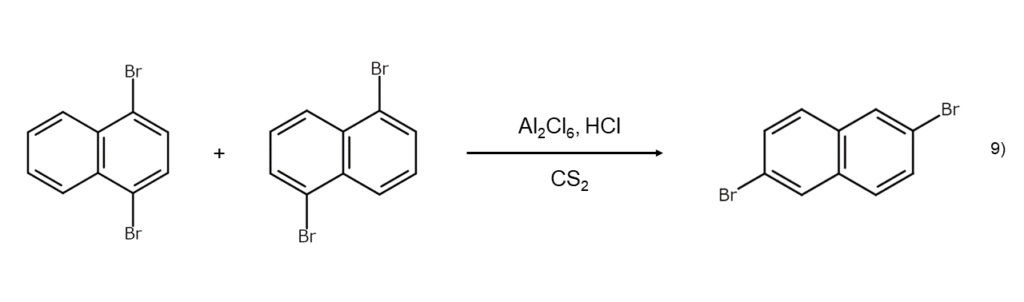
ナフタリンを二臭素化すると1,4-ジブロモナフタレンと1,5-ジブロモナフタレンの混合物が得られます。これをAl2Cl6とHClを含む二硫化水素に溶かして放置すると、分子内の臭素原子が2つとも転位して2,6-ジブロモナフタレンが得られます。Lewis酸に触媒されるこのような異性化は、直接的な臭素化では得られない化合物の合成手法として便利です。
マナックは、臭素化・ヨウ素化反応における世界的なリーディングカンパニーです。臭素化・ヨウ素化反応にお困りの方は、お気軽にお問い合わせください。
参考文献
1) 鈴木仁美 監修、マナック(株)研究所 著、「臭素およびヨウ素化合物の有機合成 試薬と合成法」、丸善出版
2) Nobuta, T., Hirashima, S. et al. Tetrahedron Lett., 2010, 51, 4576.
3) Terent’ev, A. O., Khodykin, S. V. et al., Synthesis, 2006, 1087.
4) Gavara, L., Boisse, T. et al. Tetrahedron, 2008, 64, 4999.
5) Koenigs, Z., Gerdes, H. C. et al. Chem. Ber., 1928, 61, 1027.
6) den Hertog, H. J., Jouwersma, C. et al. Rec. trav. chim. Pays-Bas, 1949, 68, 275.
7) den Hertog, H. J., Schogt, J. C. M. et al. Rec. trav. chim. Pays-Bas, 1950, 69, 673; ibid., 1951, 70, 353.
8) Meerwein, H., Hofmann, P. et al. J. prakt. Chem., 1940, [2], 154, 266.
9) Salkind, J., Stetzuro, Z. Chem. Ber., 1931, 64, 953.