アルケンのヨウ素付加:脂肪族化合物のヨウ素化反応②:臭素化・ヨウ素化反応解説シリーズ 19
マナックが得意とする、臭素化・ヨウ素化反応について解説する本シリーズ。前回から、「単体ヨウ素」を用いた「脂肪族化合物」のヨウ素化反応を解説しています。
今回の記事で取り上げるのは、「アルケン」に対するヨウ素の付加反応です。
前回の記事で紹介したアルカンの反応と同様に、アルケンのヨウ素化も、実はあまり効率がいい反応ではありません。だからこそ、その原理や適切な反応条件を知ることは非常に重要です。
今回も反応機構や反応例などをくわしく解説しますので、ぜひ最後までご覧ください。
■ この記事でわかること ✔ アルケンへの単体ヨウ素の付加反応は可逆性が高く、反応が遅い上に生成物が不安定で、用途が限られる ✔ イオン機構では極性溶媒や触媒を用いて進行し、ヨウ素原子以外を付加させることもでき、ラジカル機構は光や熱を利用するが、副反応が起きやすい ✔ 単体ヨウ素を他の試薬と組み合わせて使用すれば、Markovnikov型のヨウ化アルキルや逆Markovnikov型のヨウ化アルキルなど、普通なら得られない構造の生成物を得ることもできる ■ おすすめ記事 ・ アルキンのヨウ素化:脂肪族化合物のヨウ素化反応③:臭素化・ヨウ素化反応解説シリーズ 20 ・ 臭化水素を用いた臭素化反応(アルケンへの付加、アルキンへの付加):臭化水素③:臭素化・ヨウ素化反応解説シリーズ 36
contents
単体ヨウ素による脂肪族化合物のヨウ素化反応:
アルケンのヨウ素付加
反応効率が悪く、合成法としての用途は限られる
アルケンに対する単体ヨウ素の付加反応は可逆性が高く、ゆっくりとしか進行しません。さらに、生成物であるジヨードアルカンは一般に不安定で、室温でヨウ素やヨウ化水素を放出して簡単に分解してしまいます。そのため、この反応は限られた用途でしか用いられないのが現状です。
反応機構は「イオン機構」と「ラジカル機構」の2種類
アルケンと一言で言っても、その構造はさまざま。構造に応じて、付加反応の起こりやすさも当然異なります。一般には、以下の順にヨウ素付加が起こりやすいと考えられています。
CH2=CHCH3 > CH2=CHCH2OH > CH2=CH2 > CH2=CHCH2OCOCH3 > CH2=CHCH2Br
アルケンに対する単体ヨウ素の付加反応には、「イオン機構」と「ラジカル機構」の2種類があります。それぞれの詳細は以下のとおりです。
①イオン機構
イオン機構は、極性溶媒中で、ヨウ素分子間の錯形成によるイオン種の発生を経て進行します
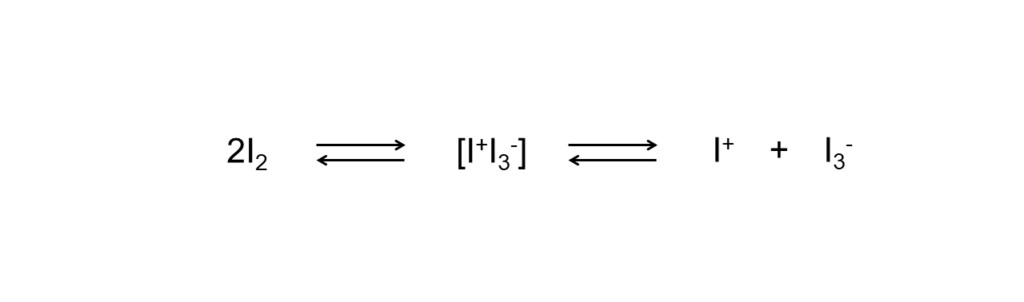
この反応はヨウ素単独では起こりにくいため、通常は触媒(酸触媒や固体表面など)を活用します。また、褐色の溶液(酢酸、アルコール、ニトロベンゼン)の方が、紫色の溶液(四塩化炭素、クロロホルム、二硫化炭素、ヘキサン)よりも付加が速く進行することが知られています。
②ラジカル機構
ラジカル機構は、気相や極性溶媒中で、熱または光励起によるヨウ素原子の発生を経て連鎖的に進行します。
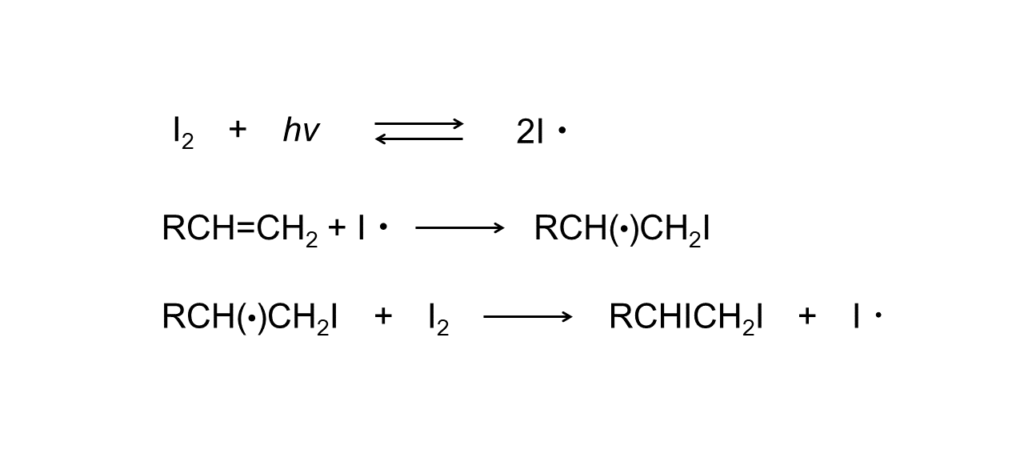
光励起の場合は、-50~-90℃の温度、4200~4500nmの光波長で反応を行うのが一般的です。しかし、光量子収率はアルケンの構造に大きく支配されるため、反応ごとに条件を検討する必要があります。
さらに無視できないのが、副反応による影響です。紫外光を使用する場合や室温で反応を行う場合には、アルケンの重合や生成物の光分解が優先されるため、ヨウ素付加による生成物がうまく得られません。
例えば、スチレンやブタジエンに室温で単体ヨウ素を作用させると、付加反応ではなく重合反応がはじまってしまいます。また、アリルアルコールに単体ヨウ素を作用させた場合は、付加反応が起こり2,3-ジヨードプロパノールの結晶が分離しますが、この結晶はすぐに分解して暗色の物質に変化してしまいます。
イオン機構:ヨウ素原子以外を付加させることも可能
イオン機構の場合、反応条件を工夫すれば、さまざまな官能基をもつヨードアルカンを得ることが可能です。
①メタノールや酢酸などに対応する官能基を導入する
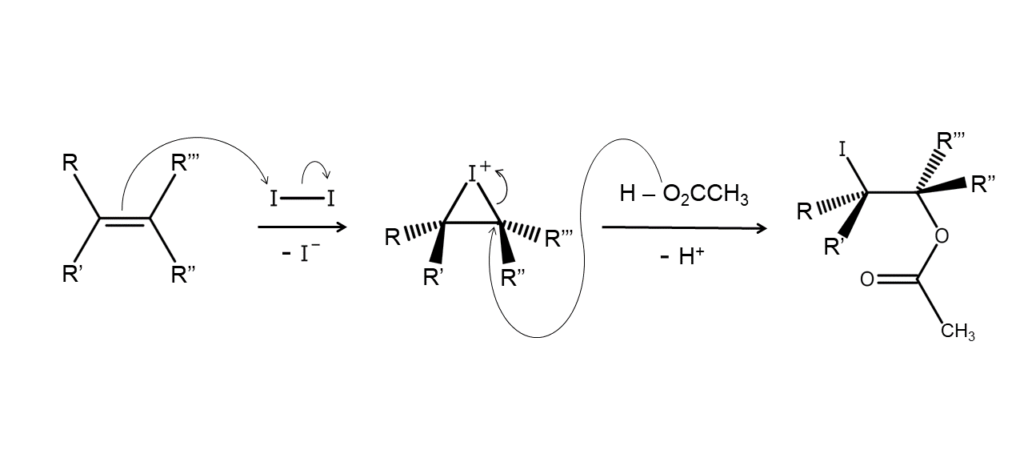
極性溶媒中で、求核種の共存下にアルケンへ単体ヨウ素を作用させます。すると、ヨウ素が1つ付加して生成した環状ヨードニウムイオン中間体が求核種によって捕捉され、求核種に対応する官能基をもつヨードアルカンが得られます。
求核種としてよく使用されるのは、メタノール、酢酸、アルキルアミンなどです。
②次亜ヨウ素酸やその誘導体に対応する官能基を導入する
水、アルコール、またはカルボン酸を溶媒として、アルケンへ単体ヨウ素を作用させます。すると系中には、次亜ヨウ素酸(HOI)、次亜ヨウ素酸のアルキル誘導体(ROI)、次亜ヨウ素酸のアシル誘導体(RCOOI)がそれぞれ生成します。これらがアルケンをヨードヒドロキシ化、ヨードアルコキシ化、またはヨードアシル化することで、対応するヨウ化物(ヨードヒドリンやその誘導体)が生成するのです。
この反応も、①と同じくヨードニウムイオン中間体を経由して進行します。系中のHOI、ROI、RCOOIはヨードニウムイオン中間体を攻撃する求核種として働くとともに、ヨードニウムイオン中間体自体を円滑に生成させる役割も果たします。
また、ヨードヒドリン誘導体を合成する場合は、穏やかな酸化剤や酸触媒を併用すると好結果が得られるケースが多いようです。
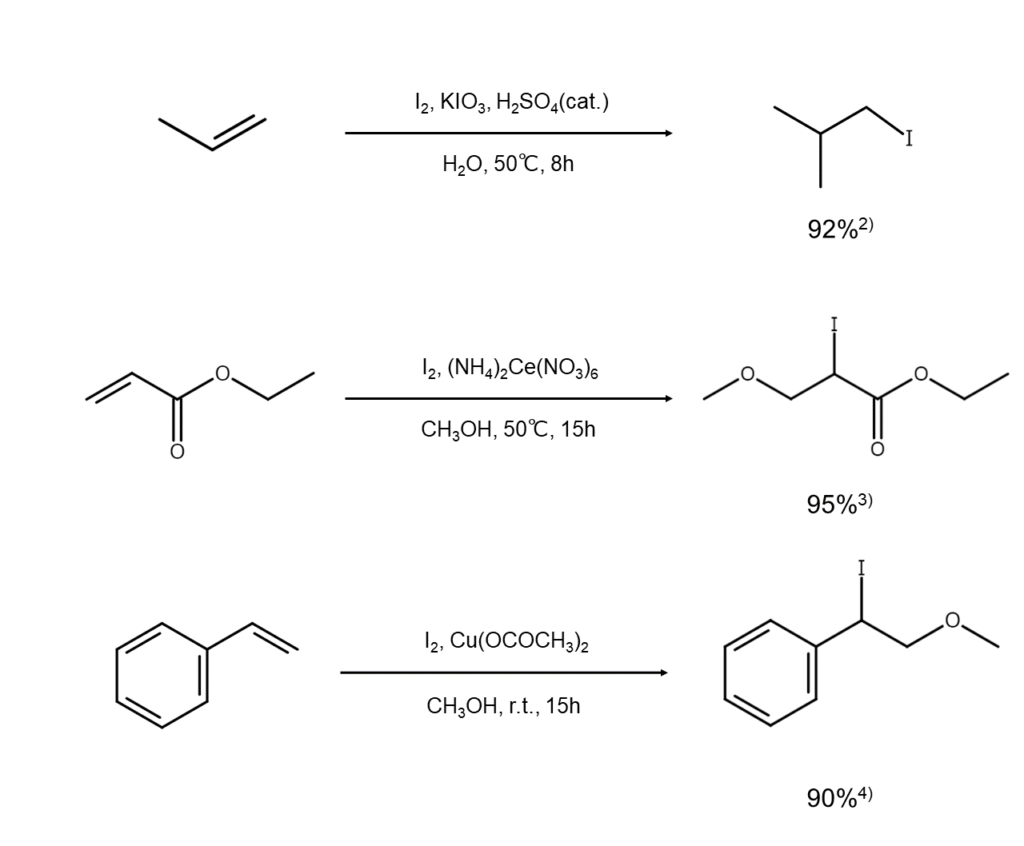
以下に、溶媒として水またはメタノールを使用した反応例を示します。
③フッ素を官能基として導入する
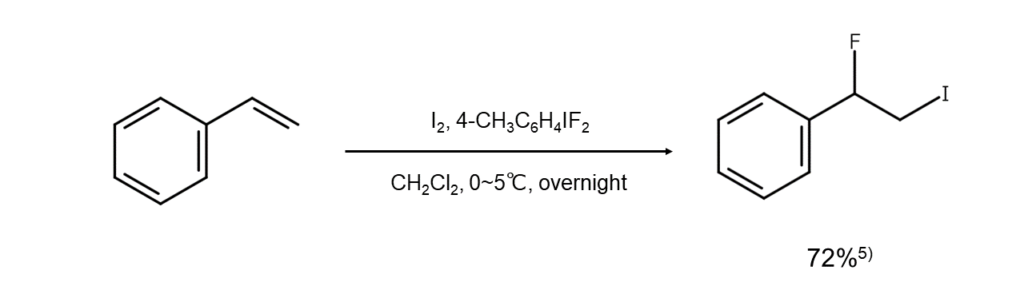
単体ヨウ素とともに、高原子価ヨウ素試薬である4-ヨードトルエンジフルオリド4-CH3C6H4IF2を用いると、ヨードフルオロ化が進行してフッ素官能基が導入されます。この反応は、フッ素アニオンF–が求核種としてヨードニウムイオン中間体を攻撃することで進行すると推定されています。
反応例は以下のとおりです。
イオン機構:γ~ε位にオレフィン結合がある場合は、ヘテロ環化合物の合成もできる
γ~ε位にオレフィン結合をもつアルコールやチオール、カルボン酸などと単体ヨウ素を反応させた場合、発生した環状ヨードニウムイオン中間体が分子内のヘテロ元素官能基(ヒドロキシル基など)からSN2攻撃を受けて、対応する環状エーテル、環状スルフィド、ラクトンが好収率で得られます。
この形式の反応は、基質の構造をうまく工夫すれば複雑な骨格を1段階で構築できるため、医薬品や天然物関連のヘテロ環合成にも広く利用されています。代表的な反応例は以下のとおりです(他の反応例についても知りたい方は、本記事末尾の参考文献7)〜10)をご覧ください)。
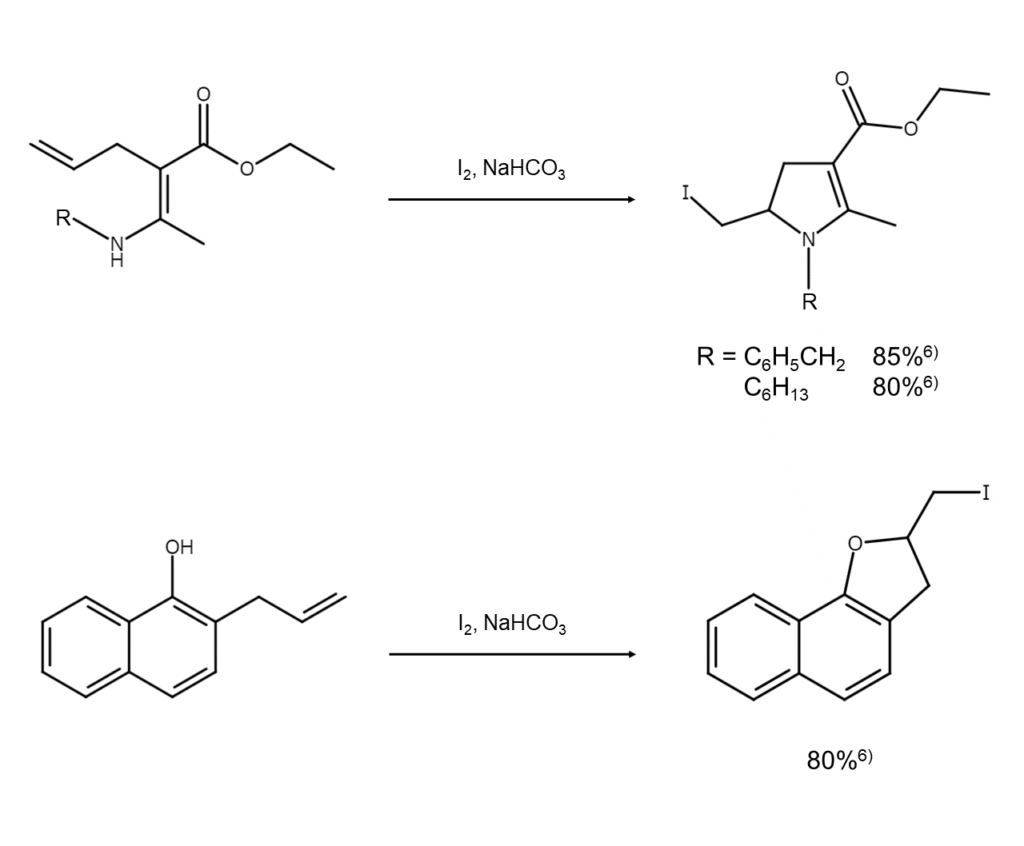
アルキル側鎖上にヨウ素官能基をもつこれらのヘテロ環化合物は一般に反応性が高いため、加熱したり長期間保存したりすると、HIを放出して重合しやすくなってしまいます。重合が起こらないよう、適切に管理することが重要です。
また、これらのヘテロ環化合物には皮膚を強く刺激するものが多いため、触れてはいけません。取り扱いには十分に注意しましょう。
【コラム】 ヒドロホウ素化と単体ヨウ素を使えば、逆Markovnikov付加も可能
単体ヨウ素を他の試薬と組み合わせて使用すれば、普通なら得られない構造の生成物を得ることも可能です。今回は、その一例をご紹介しましょう。
アルケンにHIを付加させる場合、通常は以下のように、より安定なカルボカチオン中間体を経由するMarkovnikov型のヨウ化アルキルが得られます。
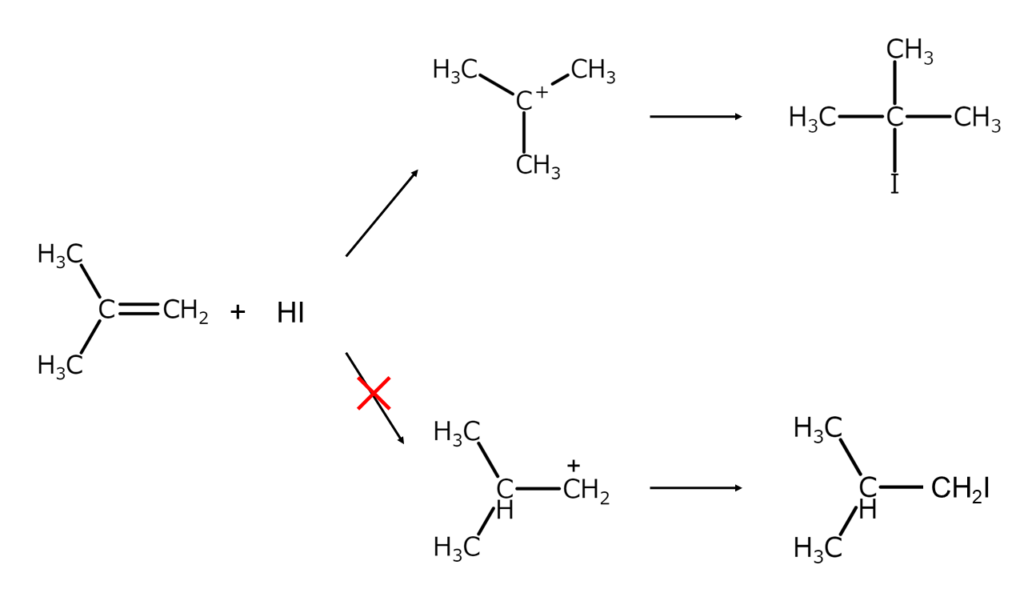
それでは、逆Markovnikov型のヨウ化アルキルを得たい場合はどうすればいいのでしょうか?この問題を解決するのが、「ヒドロホウ素化」と「単体ヨウ素」です。
アルケンをボランでヒドロホウ素化してトリアルキルボラン(R3B)に変えたのち、これを単体ヨウ素で処理(ヨウ素化分解)すれば、逆Markovnikov型の生成物が得られます。R3Bのような有機ホウ素は一般に単体ヨウ素との反応が遅いため、通常は水酸化ナトリウムやナトリウムメトキシドのような強アルカリを作用させていったんボロン酸塩に変えたのち、これを単体ヨウ素で開裂させます。反応式は以下のとおりです。
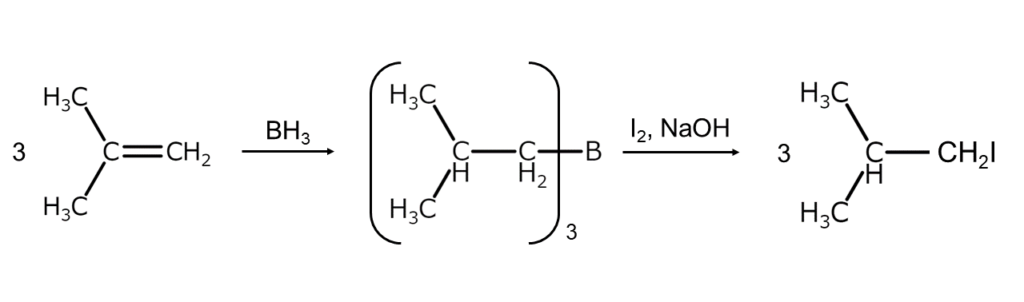
逆Markovnikov付加した化合物が必要な場合は、ぜひ上記の反応を試してみてください。
参考文献
1) 鈴木仁美 監修、マナック(株)研究所 著、「臭素およびヨウ素化合物の有機合成 試薬と合成法」、丸善出版
2) Cornforth, J. W., Green, D. T. J. Chem. Soc. C, 1970, 846.
3) Horiuchi, C. A., Ochiai, K. et al. Chem. Lett., 1994, 185.
4) Georgoulis, C., Valery, J. M. Synthesis, 1978, 402.
5) Conte, P., Panunzi, B. et al. Tetrahedron Lett., 2006, 47, 273.
6) Pacote, C. G., de Carvalho, B. S. et al. Synthesis, 2009, 3963.
7) Dowle, M. D., Davies, D. I. Chem. Soc. Rev., 1979, 8, 171.
8) Cardillo, G., Orena, M. Tetrahedron, 1990, 46, 3321.\
9) Robin, S., Rousseau, G. Tetrahedron, 1998, 54, 13681.
10) Ranganathan, S., Muraleedharan, N. K. et al. Tetrahedron, 2004, 60, 5273.