ハロゲン化試薬として使える! 超原子価有機ヨウ素化合物の概要と、ジハロゲノヨード化合物を解説:超原子価有機ヨウ素化合物①:臭素化・ヨウ素化反応解説シリーズ 29
Chemiaでは、マナックが得意とする、臭素化・ヨウ素化反応について解説してきました。今回からは、「超原子価有機ヨウ素化合物」を取り上げます。
「超原子価有機ヨウ素化合物」とは耳慣れない名前ですが、一体どのような性質の化合物なのでしょうか。そして、どのような用途に使われているのでしょうか。実は、超原子価有機ヨウ素化合物には、すばらしいメリットがたくさんあります。これから数回にわたり、その秘密をひもといていきます。
初回はまず、超原子価有機ヨウ素化合物の概要を説明し、その一種である(ジハロゲノヨード)化合物の特徴や反応を説明します。ぜひ、最後までお楽しみください。
contents
超原子価有機ヨウ素化合物とは
超原子価状態をとるヨウ素を含む有機化合物
「超原子価有機ヨウ素化合物」は、名前のとおり「超原子価」を持つ「有機ヨウ素化合物」です。
「超原子価」とは、ある原子の原子核から最も遠く離れた電子殻(ほかの原子との結合に関係する部分)が形式的に8つ以上の電子を持つことで、ほかの原子との間により多くの結合が形成できるようになった状態をいいます。例えばヨウ素原子は、超原子価状態になると、下図のように複数の原子と結合できるようになります(下図左側のヨウ素原子は三価、右側のヨウ素原子は五価の状態)。このような超原子価状態をとるヨウ素を含む有機化合物が、「超原子価有機ヨウ素化合物」なのです。
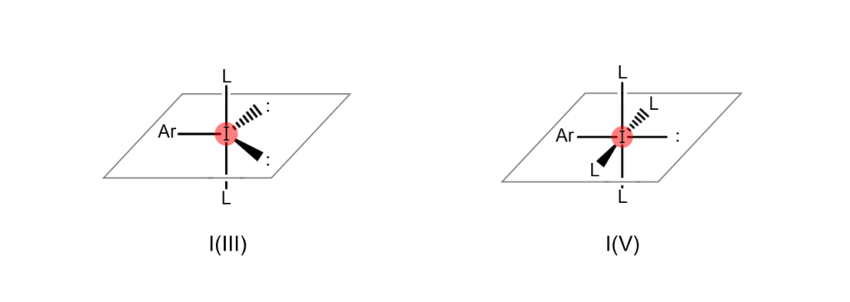
かつて、実験室で手にする有機ヨウ素化合物はほとんどが一価のものでした。しかし近年、上記のような超原子価化合物が多く合成されるようになり、一部は試薬として市販されています。
よく知られている超原子価有機ヨウ素化合物には、(ジクロロヨード)ベンゼン、(ジアセトキシヨード)ベンゼン、ヨードシルベンゼン、ヨージルベンゼンなどがあります。
酸化剤や脱水素材、有害元素の代替試薬などとして活躍
超原子価有機ヨウ素化合物は、実験室で、穏和な酸化剤、脱水素剤、官能基の導入試薬などとして利用されてきました2)。
また、超原子価有機ヨウ素化合物は化学的に有機水銀(II)、有機タリウム(III)、有機鉛(IV)などの化合物と類似した挙動を示すことが多いので、これらの有害元素の代替試薬としても使用できます。さらに、超原子価ヨウ素の優れた脱離性を利用したアルキル化およびアリール化剤として、近年、ポリフルオロアルキルヨードニウム、アルキニルヨードニウム、ジアリールヨードニウムなどのヨードニウム塩が比較的安価で市販されています。
超原子価有機ヨウ素化合物についてくわしく学びたい方へ
これから数回にわたり、さまざまな超原子価有機ヨウ素化合物の特徴や反応を解説していきます。しかし、記事を読む過程で「もっとくわしく知りたいな……」と思うこともあるかもしれません。その場合は、本記事末尾の参考文献2)~14)として紹介している参考書や総説にも目を通してみてください。
超原子価ヨウ素化合物の紹介:(ジハロゲノヨード)化合物
(ジクロロヨード)アレーン
ジクロロヨードアレーンは、黄色~オレンジ色の結晶です。通常の条件下では安定に扱える場合が多いものの、加熱したり日光に当てたりすると速やかに分解します。また、冷暗所でも徐々に分解するため、長期保存には適していません。
ジクロロヨードアレーンの合成方法としては、クロロホルム中でヨードアレーンに塩素を作用させ、ヨウ素原子を酸化させる方法が知られています15)。また、ヨードアレーンを過ホウ素酸ナトリウム16)、過硫酸ナトリウム17)、塩素酸カリウム18)、酸化クロム19)などの酸化剤の共存下で酸と反応させる方法もあります。合成例は以下のとおりです。
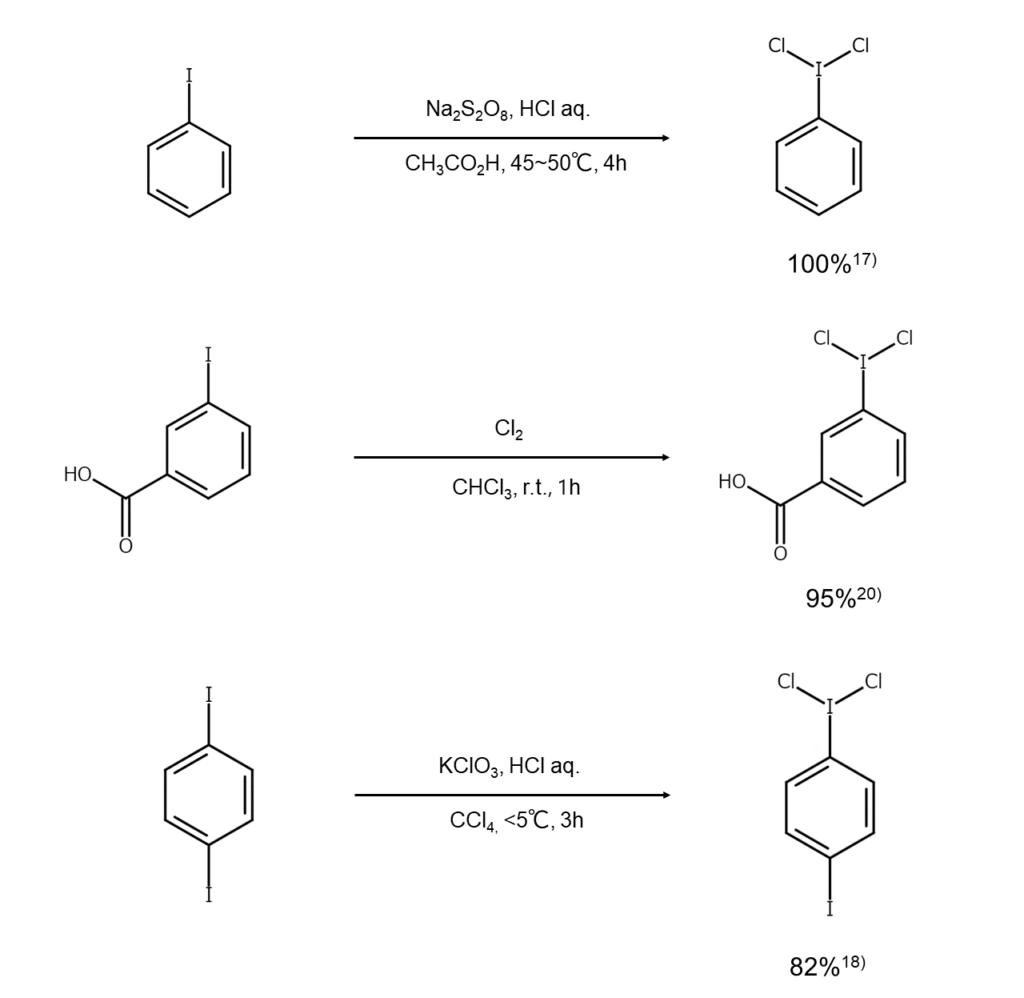
ジクロロアレーンは、実験室では穏やかな塩素化剤として利用されます。ジクロロアレーンを用いてアルケンへの塩素付加反応を行うと、イオン反応条件下ではtrans体、ラジカル反応条件下ではcis/trans体の混合物が得られます。また、ジクロロアレーンを希NaOH水溶液で加水分解すると、ヨードシルアレーンに変化します21)。
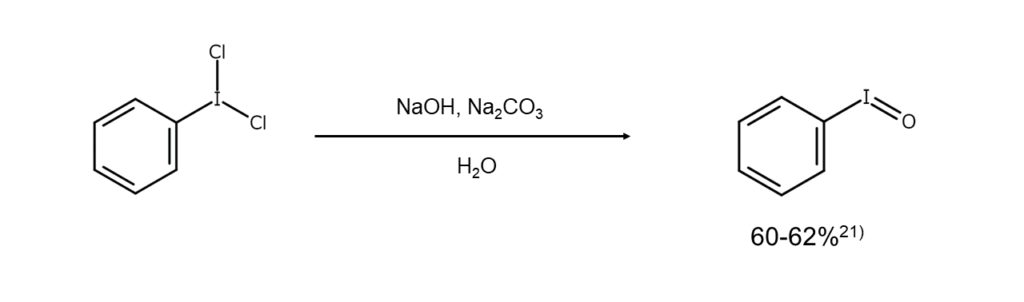
(ジフルオロヨード)アレーン
(ジフルオロヨード)アレーンは、アルケン、カルボニル化合物、ヨードアルカンなどのフッ素化に利用される化合物です。
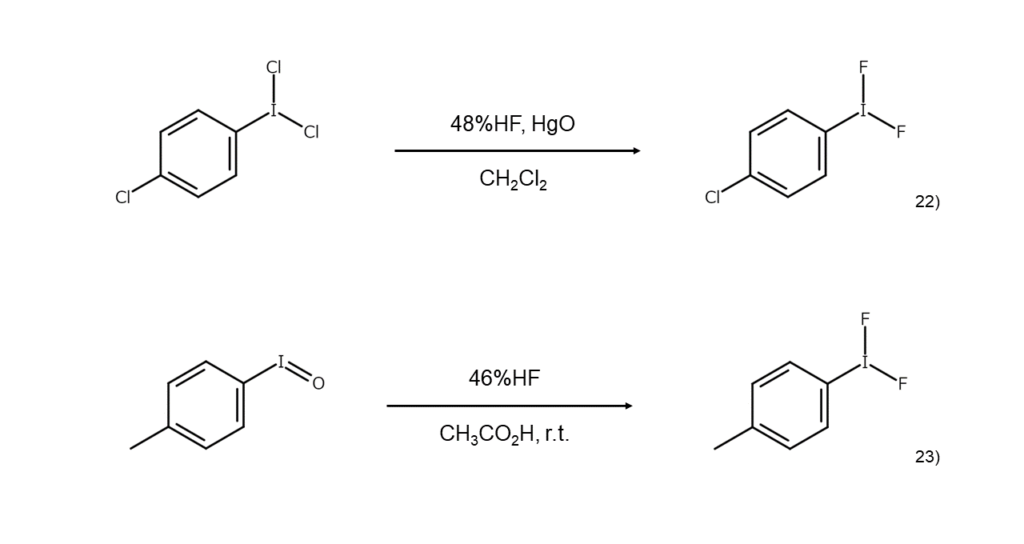
(ジフルオロヨード)アレーンの合成法としては、HgOの存在下で(ジクロロヨード)アレーンにフッ化水素酸を作用させる方法22)、ヨードシルアレーンをフッ化水素酸23)やSF424)で処理する方法、トリエチルアミン・3フッ化水素[(C2H5)3N・3HF]の共存下でヨードアレーンを電気化学的に酸化する方法などが知られています25)。
【コラム】超原子価ヨウ素化合物の命名法って?
今回紹介した三価と五価のヨウ素化合物は、それぞれ仮想の水素化物である「ヨージナン:H3I」と「ペルヨージナン:H5I」の誘導体として慣用的に命名されてきました。しかし、IUPAC(国際純正応用化学連合)は基準化合物をヨウ化水素HIとし、これをヨーダン(iodane)と呼ぶ新しい命名法を提唱しています。
IUPACの命名法では、基準結合数を超える化合物はその数値をλの肩番号として示すことになっています。これにしたがうと、先ほどの「ヨージナン」は「λ3-ヨーダン」、「ペルヨージナン」は「λ5-ヨーダン」となります。
ところが、このIUPACが提唱する新しい命名法は、まだ当該分野の研究者たちにさえあまり使用されていないようです。そのため、この記事では従来の名称や慣用名を使用しています。
とは言え、新しい命名法を理解しておけば文献の調査範囲も広がるでしょうし、状況に応じて命名法を使い分けることもできるはずです。可能なら、慣用名と新しい命名法の両方を理解しておきたいですね。
マナックは、超原子価有機ヨウ素化合物の製造・販売を承っています。特に、DAIB((ジアセトキシヨード)ベンゼン)は大幅な製造コスト削減に成功していますので、高品質な製品を低コストで提供することが可能です。
以下のメールアドレスまで、ぜひお気軽にお問い合わせください。
chemia@manac-inc.co.jp
参考文献
1) 鈴木仁美 監修、マナック(株)研究所 著、「臭素およびヨウ素化合物の有機合成 試薬と合成法」、丸善出版
2) Willgerodt, C. Die organischer Verbindungen mit mehrwertigen Jod, Ferdinand Enke (1914).
3) Sandin, R. B. Chem. Rev., 1943, 32, 249.
4) Beringer, F. M., Gindler, E. M. Iodine Abstract Rev., 1956, 3, 70.
5) Banks, D. F. Chem. Rev., 1966, 66, 243.
6) Varvoglis, A. Chem. Soc. Rev., 1981, 10, 377.
7) Varvoglis, A. Hypervalent Iodine Chemistry (Top. Curr. Chem. 224), Springer (2003).
8) Merkushev, E. B., Schwarzberg, M. C. Organoiodine Compounds in Organic Synthesis, Tomsk Ped. Inst. Tomsk, USSR (1978).
9) Varvoglis, A. Synthesis, 1984, 709.
10) Varvoglis, A. The Organic Chemistry of Polycoordinated Iodine VCH, New York (1992).
11) Wirth, T., Hirt, U. H. Synthesis, 1999, 1271.
12) Stang, P. J., Zhdankin, V. V. Chem. Rev., 1996, 96, 1123.
13) Zhdankin, V. V., Stang. P. J. Chem. Rev., 2002, 102, 2523.
14) Zhdankin, V. V., Stang. P. J. Chem. Rev., 2008, 108, 5299.
15) Lucas, H. J., Kennedy, E. R. Org. Synth. Coll. Vol. III, 482 (1955).
16) Koyuncu, D., McKillop, A. et al. J. Chem. Res. (S), 1990, 21.
17) Baranowski, A., Plachta, D. et al. J. Chem. Res. (S), 2000, 435.
18) Krassowska-Swiebocka, B., Prokopienko, G. et al. Synlett, 1999, 1409.
19) Kazmierczak, P., Skulski, L. J. Chem. Res. (S), 1999, 64.
20) Yusubov, M. S., Drygunova, L. A. et al. Synthesis, 2004, 2289.
21) Lucas, H. J., Kennedy, E. R. Org. Synth. Coll. Vol. III, 483 (1955).
22) Carpenter, W. J. Org. Chem., 1966, 31, 2688.
23) Garvey, Jr., B. S., Halley, L. F. et al. J. Am. Soc. Chem., 1937, 59, 1827.
24) Lyalin, V. V., Orda, V. V. et al. Zn. Org. Khim., 1970, 6, 329.
25) a) Fuchigami, T., Fujita, T. J. Org. Chem., 1994, 59, 7190. b) Fujita, T., Fuchigami, T. Tetrahedron Lett., 1996, 37, 4725.